
【题目】下列事实不能用勒夏特列原理解释的是
A. CaCO3(s) ![]() CaO(s)+CO2(g),平衡时将容器的体积缩小至一半,新平衡的CO2浓度与原平衡相同
CaO(s)+CO2(g),平衡时将容器的体积缩小至一半,新平衡的CO2浓度与原平衡相同
B. 升温Kw增加
C. 用热的纯碱溶液去污效果更佳
D. 恒温恒压的容器中有2NO2![]() N2O4,若通入Ar,气体的颜色先变浅后逐渐加深
N2O4,若通入Ar,气体的颜色先变浅后逐渐加深
【答案】A
【解析】A. CaCO3(s) ![]() CaO(s)+CO2(g),平衡时将容器的体积缩小至一半,c(CO2)增大,平衡逆向移动,根据勒夏特列原理,新平衡的CO2浓度比原平衡时大,但温度不变,平衡常数不变,K= c(CO2)不变,因此新平衡的CO2浓度与原平衡相同,不能用勒夏特列原理解释,故A选;B. 水的电离是吸热过程,升高温度,促进水的电离,Kw= c(H+)c(OH-)增加,能够用夏特列原理解释,故B不选;C.碳酸根水解CO32-+H2O
CaO(s)+CO2(g),平衡时将容器的体积缩小至一半,c(CO2)增大,平衡逆向移动,根据勒夏特列原理,新平衡的CO2浓度比原平衡时大,但温度不变,平衡常数不变,K= c(CO2)不变,因此新平衡的CO2浓度与原平衡相同,不能用勒夏特列原理解释,故A选;B. 水的电离是吸热过程,升高温度,促进水的电离,Kw= c(H+)c(OH-)增加,能够用夏特列原理解释,故B不选;C.碳酸根水解CO32-+H2O![]() HCO3-+OH-,溶液呈碱性,水解过程是吸热过程,升高温度促进碳酸根水解,碱性增强,去油污能力增强,能用勒夏特利原理解释,故C不选;D.恒温恒压的容器中有2NO2
HCO3-+OH-,溶液呈碱性,水解过程是吸热过程,升高温度促进碳酸根水解,碱性增强,去油污能力增强,能用勒夏特利原理解释,故C不选;D.恒温恒压的容器中有2NO2![]() N2O4,若通入Ar,导致容器体积增大,二氧化氮浓度降低,所以颜色变浅,但平衡逆向移动,导致气体颜色又加深,可以用平衡移动原理解释,故D不选;故选A。
N2O4,若通入Ar,导致容器体积增大,二氧化氮浓度降低,所以颜色变浅,但平衡逆向移动,导致气体颜色又加深,可以用平衡移动原理解释,故D不选;故选A。


科目:高中化学 来源: 题型:
【题目】某有机物的结构简式是: 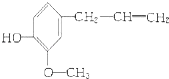 该物质不应有的化学性质是( ) ①可以燃烧
该物质不应有的化学性质是( ) ①可以燃烧
②可以跟溴加成
③可以将KMnO4酸性溶液还原
④可以跟NaHCO3溶液反应
⑤可以跟NaOH溶液反应
⑥可以发生消去反应.
A.①③
B.③⑥
C.④⑥
D.④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在相同温度下,0.01molL﹣1 NaOH溶液和0.01molL﹣1的盐酸相比,下列说法正确的是( )
A.由水电离出的[H+]相等
B.由水电离出的[H+]都是1.0×10﹣12 molL﹣1
C.由水电离出的[OH﹣]都是0.01 molL﹣1
D.两者都促进了水的电离
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于相同质量的SO2和SO3 , 下列说法:①硫元素的质量比为5:4 ②分子数之比为5:4③原子总数之比为15:16④同温同压下的两种气体体积之比为5:4.其中正确的是( )
A.①②③④
B.①②④
C.只有③
D.其它组合
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.将 100g10%的盐酸加热蒸发,得到 50 g溶液,其浓度为20%
B.把3mol/L的硫酸与等体积的水混合,所得溶液的浓度大于1.5 mol/L
C.把200mL3mol/L的BaCl2溶液跟100mL3mol/L的KCl溶液混合后,溶液中的c(Cl﹣)仍然是3 mol/L
D.已知某温度下KNO3的溶解度是 31.6 g/100 g水,在该温度下将 20 g的KNO3溶于 50 g的水中,所得溶液的质量分数是28.6%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某气态烃1mol 恰好与1molHCl加成,生成物分子中的氢又可被5molCl2完全取代,则此气态烃可能是( )
A. C4H10 B. C2H4 C. CH2=CH—CH3 D. CH2=C(CH3)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究SO2、NOx等对改善空气质量具有重要意义.
(1)NOx是汽车尾气中的主要污染物之一.①NOx能形成酸雨,由NO2形成的酸雨中含有的主要离子有 .
②汽车发动机工作时的高温会引发N2和O2反应,反应的化学方程式是 .
(2)为减少SO2的排放,常采取一些有效措施.①在含硫煤中加入生石灰可以起到固硫的作用,燃烧过程中,硫元素转化成其最高价态的化合物,该化合物的化学式是 .
②下列物质中,可用于吸收烟气中的SO2的是(填序号).
a.Na2CO3 b.H2SO4 c.NaHSO3 d.NH3H2O
(3)取某空气样本用蒸馏水处理制成待测液,其中所含的离子及其浓度如表:
离子 | K+ | Na+ | NH4+ | H+ | SO | NO | Cl﹣ |
浓度/molL﹣1 | 4×10﹣6 | 6×10﹣6 | 2×10﹣5 | a | 4×10﹣5 | 3×10﹣5 | 2×10﹣5 |
根据表中数据计算:a=mol/L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知H﹣H键的键能为436kJ/mol,O═O键的键能为498kJ/mol,根据热化学方程式H2(g)+ ![]() O2(g)═H2O(l)△H=﹣286kJ/mol,判断H2O分子中O﹣H键的键能为( )
O2(g)═H2O(l)△H=﹣286kJ/mol,判断H2O分子中O﹣H键的键能为( )
A.485.5 kJ/mol
B.610 kJ/mol
C.917 kJ/mol
D.1 220 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向27.2g Cu和Cu2O的混合物中加入某浓度的稀硝酸0.5L,固体物质完全反应,生成NO和Cu(NO3)2 . 在所得溶液中加入1.0molL﹣1的NaOH溶液1.0L,此时溶液呈中性,金属铜离子已完全沉淀,沉淀质量为39.2g.下列有关说法不正确的是( )
A.Cu与Cu2O的物质的量之比为2:1
B.沉淀为氢氧化铜
C.产生的NO在标准状况下的体积为4.48 L
D.Cu、Cu2O与硝酸恰好完全反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com