
| ���� | KCl | NaCl | K2Cr2O7 | Na2Cr2O7 | |
| �ܽ�� ��g/100gˮ�� | 0�� | 28 | 35.7 | 4.7 | 163 |
| 40�� | 40.1 | 36.4 | 26.3 | 215 | |
| 80�� | 51.3 | 38 | 73 | 376 | |
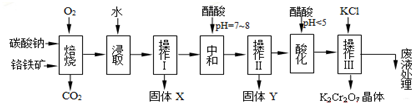
���� ������ͨ�����գ������ķ�Ӧ��4FeO•Cr2O3+8Na2CO3+7O2 $\frac{\underline{\;750��\;}}{\;}$8Na2CrO4+2Fe2O3+8CO2����Na2CO3+Al2O3 2NaAlO2+CO2�������Եõ��Ĺ����к���Na2CrO4��Fe2O3��MgO��NaAlO2��Ȼ���ˮ�ܽ�ù���Fe2O3��MgO����ҺNa2CrO4��NaAlO2�������Թ������Һ���ù��˷������룬���Բ���I�ǹ��ˣ��õ���X�ɷ�ΪFe2O3��MgO����Һ�гɷ���Na2CrO4��NaAlO2������Һ�м�����Ტ������Һ��pHΪ7-8��ʹƫ��������ȫת��ΪAl��OH��3������Ȼ����ù��˷�����ȥ�����������������Բ���II�ǹ��ˣ��õ���YΪAl��OH��3������������Һ��pHΪС��5��ʹCrO42-ת��ΪCr2O72-�������������Һ�м����Ȼ��أ������ܽ�ȼ�С��K2Cr2O7��
��1�����������Թ������Һ���ù��˷�����
��2���ܽ�ȴ��������ת��Ϊ�ܽ��С�����ʣ�
��3������Һ�л�ȡ����ķ����ǣ�����KC1���塢����Ũ������ȴ�ᾧ�����ˡ�ϴ�ӡ����
��4����������������ǿ����Һ������Һ��ͨ�����������̼���ܽ�ƫ������ת��ΪAl��OH��3����������������������õ�Al2O3���ٸ���Alԭ���غ�����京����
��5������I2+2S2O32-=2I-+S4O62-�е��������������֮���ϵʽ���������ʵ������ٸ���Cr2O72-+6I-+14H+=2Cr3++3I2+7H2O�е��Cr2O72-֮��Ĺ�ϵʽ����Cr2O72-�������Ӷ������䴿�ȣ�
��� �⣺������ͨ�����գ������ķ�Ӧ��4FeO•Cr2O3+8Na2CO3+7O2 $\frac{\underline{\;750��\;}}{\;}$8Na2CrO4+2Fe2O3+8CO2����Na2CO3+Al2O3 $\frac{\underline{\;750��\;}}{\;}$2NaAlO2+CO2�������Եõ��Ĺ����к���Na2CrO4��Fe2O3��MgO��NaAlO2��Ȼ���ˮ�ܽ�ù���Fe2O3��MgO����ҺNa2CrO4��NaAlO2�������Թ������Һ���ù��˷������룬���Բ���I�ǹ��ˣ��õ���X�ɷ�ΪFe2O3��MgO����Һ�гɷ���Na2CrO4��NaAlO2��
����Һ�м�����Ტ������Һ��pHΪ7-8��ʹƫ��������ȫת��ΪAl��OH��3������Ȼ����ù��˷�����ȥ�����������������Բ���II�ǹ��ˣ��õ���YΪAl��OH��3������������Һ��pHΪС��5��ʹCrO42-ת��ΪCr2O72-�������������Һ�м����Ȼ��أ������ܽ�ȼ�С��K2Cr2O7��
��1�����������Թ������Һ���ù��˷�����ͨ�����Ϸ���֪������IΪ���ˣ�
�ʴ�Ϊ�����ˣ�
��2���ܽ�ȴ��������ת��Ϊ�ܽ��С�����ʣ����ݱ�������֪������������K2Cr207���ܽ����С��Na2Cr207���ܽ�ȱ�K2Cr207����������Һ���ܷ�����ӦNa2Cr207+2KCl=K2Cr207��+2NaCl��
�ʴ�Ϊ��K2CrO7 ���ܽ�ȱ�Na2Cr2O7С��
��3������Һ�л�ȡ����ķ����ǣ�����KC1���塢����Ũ������ȴ�ᾧ�����ˡ�ϴ�ӡ����
�ʴ�Ϊ����ȴ�ᾧ��ϴ�ӣ�
��4����������������ǿ����Һ�������ܽ������������Լ���NaOH��Һ������Һ��ͨ�����������̼���ܽ�ƫ������ת��ΪAl��OH��3����������������������õ�Al2O3��n��Al2O3��=$\frac{ng}{102g/mol}$������Alԭ���غ��n[Al��OH��3]=2n��Al2O3��=$\frac{n}{51}$mol��������������������=$\frac{\frac{n}{51}mol��78g/mol}{mg}$��100%=$\frac{26n}{17m}$��100%��
�ʴ�Ϊ��NaOH��Һ��CO2�� $\frac{26n}{17m}$��100%��
��5������I2+2S2O32-=2I-+S4O62-�е��������������֮���ϵʽ��n��I2��=$\frac{0.1000mol/L��0.0474L}{2}$��1=0.00237mol���ٸ���Cr2O72-+6I-+14H+=2Cr3++3I2+7H2O��n��Cr2O72-��=$\frac{1}{3}$n��I2��=$\frac{1}{3}$��0.00237mol=0.00079mol��250mL�ظ������n��Cr2O72-��=0.0079mol��
m��K2Cr2O7��=0.0079mol��294g/mol=2.3226g��
�䴿��=$\frac{2.3226g}{2.5g}$��100%=92.9%��
�ʴ�Ϊ��92.9%��
���� ���⿼�����ʵ��Ʊ������ʺ����IJⶨ��֪ʶ�㣬Ϊ�߿���Ƶ�㣬���ؿ������������Ԫ�ػ�����֪ʶ�����������ȣ���ȷ����ͼ��ÿһ�������ķ�Ӧ�������������ѵ��ǣ�5������㣬��ȷ�ж��ظ���غ�������������֮���ϵ���ɽ����Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
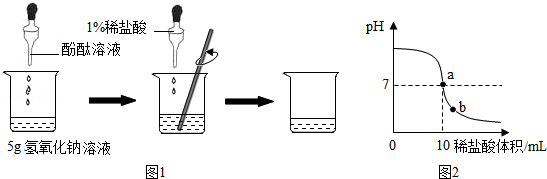
 ��֪���������ᣨH2N2O2����һ�ֶ�Ԫ�ᣬ25��ʱ����0.01mol��L-1������ζ�10mL0.01mol��L-1Na2N2O2��Һ����Һ��pH���������[V��HCl��]�Ĺ�ϵ��ͼ��ʾ���·�˵����ȷ���ǣ�������
��֪���������ᣨH2N2O2����һ�ֶ�Ԫ�ᣬ25��ʱ����0.01mol��L-1������ζ�10mL0.01mol��L-1Na2N2O2��Һ����Һ��pH���������[V��HCl��]�Ĺ�ϵ��ͼ��ʾ���·�˵����ȷ���ǣ�������| A�� | M�����Һ�м�������ˮ����Һ��pH���� | |
| B�� | N����Һ�У�c��N2O22-��+c��OH-����c��H2N2O2�� | |
| C�� | P����Һ�У�H2O���������� | |
| D�� | ��Һ��$\frac{c��{H}^{+}��}{c��H{N}_{2}{{O}_{2}}^{-}��}$��N��P��Q�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
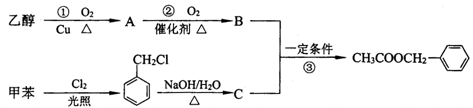
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������Ϊ20����ԭ�ӣ�${\;}_{17}^{20}$Cl | B�� | ˮ���ӵı���ģ�ͣ� | ||
| C�� | ���ԭ�ӽṹʾ��ͼ�� | D�� | Na2S�ĵ���ʽ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
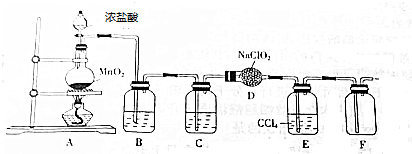
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
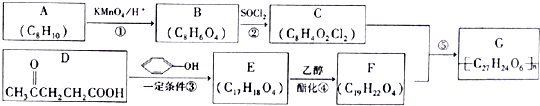
 ��
�� +HCl
+HCl ��
��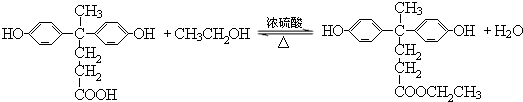 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 22.4L CO | B�� | 4.4g CO2 | C�� | 8 g SO3 | D�� | 24.5g H2SO4 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com