
【题目】下列物质的性质与应用对应关系不正确的是
A. 二氧化氯具有强氧化性,可用于杀菌消毒
B. 氢氧化铝具有弱碱性,可用于治疗胃酸过多
C. 二氧化硅的熔沸点很高,可用于制作石英坩埚
D. 钠钾合金的密度小,可用于快中子反应堆的热交换剂
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】
铁和铜都是生产、生活中应用广泛的金属,能形成很多种合金和化合物。请回答:
(1)基态Cu+的价层电子排布图为________。基态Fe3+中有________种运动状态不同的电子。
(2)铁单质能形成Fe(CO)5,其熔点为-21℃,沸点为102.8℃。则Fe(CO)5晶体的类型为________,其σ键和π键的数目之比为________。与CO互为等电子体的离子符号为________(任写一种)。
(3)铜元素的焰色反应呈绿色,很多金属元素能发生焰色反应的微观原因为________。
(4)[Cu(NH3)4]SO4中,所含基态非金属原子的第一电离能由小到大的顺序为________。阴离子的空间构型为________,其中心原子的杂化轨道类型为________。
(5)铁单质的一种晶体的堆积模型为体心立方堆积,晶胞参数为apm;铜单质的一种晶体的堆积模型为面心立方最密堆积,晶胞参数为bpm。则两种晶体中,铁原子和铜原子的配位数之比为________,晶体的密度之比为________(用代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某无色透明溶液中,下列离子一定能共存的是( )
A.H+ Cu2+ Cl﹣ SO42﹣
B.HCO3﹣ NO3﹣ Na+ H+
C.SO42﹣ Cl﹣Na+ K+
D.Na+SO42﹣H+ AlO2﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值,下列有关叙述不正确的是( )
A.标准状况下,1L庚烷所含有的分子数为![]()
B.1mol甲基(-CH3)所含电子数为9NA
C.标准状况下,B2H6和C2H4的混合气体22.4L,所含的电子数为16NA
D.26g C2H2和苯蒸气的混合气体中所含的C原子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是四种常见的短周期主族元素,其原子半径随原子序数的变化如图所示。已知Y、Z两种元素的单质是空气的主要成分,W原子的最外层电子数与Ne原子的最外层电子数相差1。下列说法正确的是

A. Y、Z、W处于同一周期
B. X、Y、Z、W的原子序数递增
C. X、W可形成化学式为XW的离子化合物
D. 简单离子半径是Z小于W
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水中有取之不尽的化学资源,从海水中可提取多种化工原料,下图是某化工厂对海水资源综合利用的示意图:
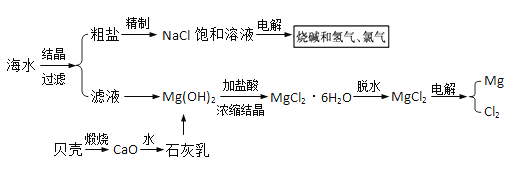
试回答下列问题:
(1)实验室里将粗盐制成精盐的过程中,过滤的操作需用到玻璃棒,玻璃棒的作用是:____,还需要的玻璃仪器有:____。
(2)粗盐中含有Ca2+、 Mg2+、 SO42-等杂质,精制后可得NaCl饱和溶液,精制时通常在溶液中:①加入过量的BaC12溶液,②过量的NaOH溶液,③过量的Na2C03溶液,则添加试剂顺序为____(填写序号),最后在滤液加入盐酸至溶液呈中性。请写出加入盐酸后可能发生反应的离子方程式:____。
(3)海水提取食盐后的母液中有K+、Na+、Mg2+等阳离子。从离子反应的角度考虑,在母液里加入石灰乳发生反应的离子方程式:____。
(4)电解无水氯化镁制取镁的化学方程式为____。将镁蒸气冷却后即为固体镁,镁蒸气需在Ar气氛围中冷却,理由:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①RNH2+R′CH2Cl![]() RNHCH2R′+HCl(R和R′代表烃基)
RNHCH2R′+HCl(R和R′代表烃基)
②苯的同系物能被高锰酸钾氧化,如: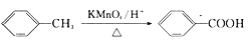
③
化合物C是制取消炎灵(祛炎痛)的中间产物,其合成路线如图所示:
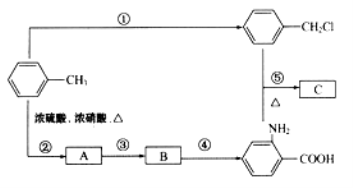
(1)B物质的结构简式是_____________.
(2)写出反应①、②的化学方程式:
①_____________________
②_____________________
(3)反应①~⑤中,属于取代反应的是_____________(填反应序号)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com