
【题目】25℃时,下列有关溶液中微粒的物质的量浓度关系错误的是( )
A.0.1mol/LCH3COONa与0.1mol/LHCl溶液等体积混合:c(Na+)=c(Cl﹣)>c(CH3COO﹣)>c(OH﹣)
B.0.1mol/LNa2CO3与0.1mol/LNaHCO3溶液等体积混合:2c(Na+)=3c(CO ![]() )+3c(HCO3﹣)+3c(H2CO3)
)+3c(HCO3﹣)+3c(H2CO3)
C.Na2C2O4溶液与HCl溶液等体积混合(H2C2O4是二元弱酸):2c(C2O ![]() )+c(HC2O
)+c(HC2O ![]() )+c(OH﹣)+c(Cl﹣)=c(Na+)+c(H+)
)+c(OH﹣)+c(Cl﹣)=c(Na+)+c(H+)
D.0.1mol/LNH4Cl与0.1mol/L氨水溶液等体积混合:c(NH3?H2O)>c(NH ![]() )>c(Cl﹣)>c(OH﹣)
)>c(Cl﹣)>c(OH﹣)
【答案】D
【解析】解:A.0.1mol/LCH3COONa与0.1mol/LHCl溶液等体积混合,生成等物质的量CH3COOH和NaCl,钠离子与氯离子不水解,二者的浓度相同,即c(Na+)=c(Cl﹣),CH3COOH是弱酸在溶液中部分电离,所以c(Na+)=c(Cl﹣)>c(CH3COO﹣)>c(OH﹣),故A正确;B.0.1mol/LNa2CO3与0.1mol/LNaHCO3溶液等体积混合,钠离子的总浓度是C的最浓度的1.5倍,所以溶液中:2c(Na+)=3c(CO ![]() )+3c(HCO3﹣)+3c(H2CO3),故正确;
)+3c(HCO3﹣)+3c(H2CO3),故正确;
C.Na2C2O4溶液与HCl溶液等体积混合(H2C2O4是二元弱酸)生成等物质的量浓度的NaHC2O4和NaCl,溶液中存在电荷守恒为:2c(C2O ![]() )+c(HC2O
)+c(HC2O ![]() )+c(OH﹣)+c(Cl﹣)=c(Na+)+c(H+),故C正确;
)+c(OH﹣)+c(Cl﹣)=c(Na+)+c(H+),故C正确;
D.0.1mol/LNH4Cl与0.1mol/L氨水溶液等体积混合,溶液显碱性,NH3H2O的电离程度大于NH4+的水解程度,所以溶液中c(NH ![]() )>c(Cl﹣)>c(NH3H2O)>c(OH﹣),故D错误.
)>c(Cl﹣)>c(NH3H2O)>c(OH﹣),故D错误.
故选D.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】某同学设计如下元素周期表,以下说法正确的是
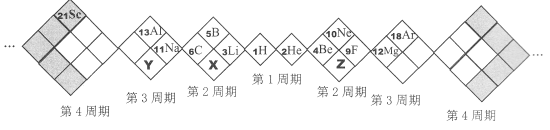
A. X、Y、Z元素分别为N、P、O
B. 所列元素都是主族元素
C. 原子半径:Z>X>Y
D. 稳定性:X的氢化物 < Y的氢化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的定容容器中,发生反应:2A(g)+B(s)C(g)+D(g),下列描述中能表明反应已达到平衡状态的是( ) ①混合气体的压强不变
②混合气体的密度不变
③C(g)的物质的量浓度不变
④容器内A,C,D三种气体的浓度之比为2:1:1
⑤单位时间内生成n molC,同时生成n mol D
⑥单位时间内生成n molD,同时生成2n mol A.
A.①②⑤
B.②③④
C.②③⑥
D.①③⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
①离子化合物中一定含离子键,也可能含共价键
②共价化合物中可能含离子键
③含金属元素的化合物不一定是离子化合物
④由非金属元素组成的化合物一定是共价化合物
⑤构成单质分子的粒子不一定存在共价键
⑥不同元素组成的多原子分子里的化学键一定是极性键
⑦有化学键断裂的变化属于化学变化
A. ①③⑤ B. ②④⑥ C. ①③④ D. ③⑤⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z为原子序数依次增大的短周期主族元素,三种元素属于不同周期。下列转化关系中,A、B、C是X、Y、Z对应的三种气态单质,其余均为常见化合物。下列分析正确的是()
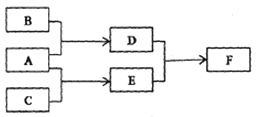
A. 离子半径;Y>Z B. Z的含氧酸均为强酸
C. 与Y同周期氢化物中D最稳定 D. F含离子键和共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、X是中学常见的无机物,存在如图转化关系(部分生成物和反应条件略去)。
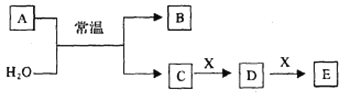
(1)若A为常见的金属单质,焰色反应呈黄色,X能使品红溶液褪色,写出C和E反应的离子方程式:___________。
(2)若A为短周期元素组成的单质,该元素的最高价氧化物的水化物酸性最强,则:
①组成单质A的元素在周期表中的位置为___________。
②A与H2O反应的离子反应方程式为______。
(3)若A为淡黄色粉末,问答下列问题:
①1molA与足量的H2O充分反应时转移的电子数目为________。
②A中所含有的化学键类型为_______。
③若X为一种造成温室效应的气体.则鉴别等浓度的D、E两种溶液,可选择的试剂为____(填代号)。
a.盐酸 b.BaCl2溶液 c.NaOH溶液 d.Ca(OH)2溶液
(4)若A为氧化物,X是Fe,溶液D中加入KSCN溶液变红。则A与H2O反应的化学反应方程式为_________,E是___________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E都是元素周期表中前20号元素,原子序数依次增大,A是地壳中含量最高的元素,B、C、D同周期,E和其他元素既不在同一周期也不在同一主族,D的氢化物及其最高价氧化物对应的水化物均为强酸,且B、C、D的最高价氧化物对应的水化物两两混合均能发生反应生成盐和水。据此回答下列问题:
(1)A和D的氢化物中,沸点较低的是 (选“A”或“D”)。
(2)元素C在元素周期表中的位置是 ,B的最高价氧化物对应的水化物的电子式为 。
(3)A、D、E可以形成多种盐,其中一种盐中A、D、E三种元素的原子个数比为2:2:1,该盐的名称为 。它的水溶液与D的氢化物的水溶液反应可生成D的单质,该反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用下列实验装置不能完成相应实验的是( )
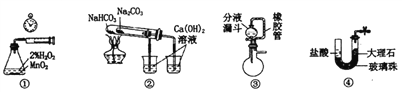
A. 用装置①测量生成氧气的化学反应速率
B. 用装置②比较NaHCO3和Na2CO3的热稳定性
C. 装置③中分液漏斗内的液体可顺利加入蒸馏烧瓶
D. 装置④可实现制取CO2实验中的“即关即止,即开即用”的作用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图实验装置用于验证某些物质的性质.在试管A中装入足量的固体NaHCO3.试回答下列问题:
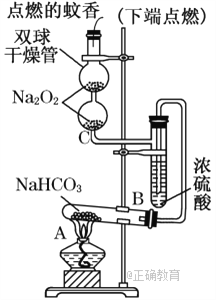
(1)在A试管内发生反应的化学方程式是____________________________________.
(2)B装置的作用是_______________________________________________________.
(3)在双球干燥管内发生反应的化学方程式为___________________________________.
(4)双球干燥管内观察到的实验现象是_________________________________________.上述实验现象说明________________________________________________________.
(5)若将干燥管内的Na2O2换成Na2O,则双球干燥管内观察到的实验现象是______________________________________________________________________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com