
| A、稀硝酸具有氧化性,可用于清洗做银镜反应的试管 |
| B、BaSO4、BaCO3均难溶于水,都可用作钡餐 |
| C、铝合金的大量使用归功于人们能用焦炭等还原剂从氧化铝中获取铝 |
| D、加热盛有NH4Cl固体的试管,管口有固体凝结,这是升华现象 |


科目:高中化学 来源: 题型:
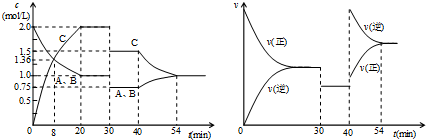
| A、30min时降低温度,40min时充入生成物C |
| B、0~8min内A的平均反应速率为0.08mol/(L?min) |
| C、反应方程式中的x=1,正反应为吸热反应 |
| D、20min~40min间该反应的平衡常数均为8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子半径的大小顺序为:X>Y>Z>Q |
| B、离子半径的大小顺序为:Xm+>Yn+>Zm->Qn- |
| C、m+a=d-n |
| D、b-n=c+m |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③④⑤ | B、②③④⑥ |
| C、①②⑥ | D、②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在非标准状况下,1 mol O2的体积也有可能是22.4 L |
| B、在温度和压强一定时,气态物质的体积主要由气体分子数目和分子的大小决定 |
| C、同温同压下,0.3 mol N2和0.7 mol O2的体积比为3:7 |
| D、同温同压下,相同体积的任何气体所含有的分子数目一定相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol乙基(-C2H5)中含有的电子数为17NA |
| B、标准状况下,22.4L氯仿(三氯甲烷)中共价键数目为4NA |
| C、1L pH=1的稀硫酸中有0.2 NA个H+ |
| D、78gNa2O2中含有2NA个阴离子(相对原子质量:Na-23 O-16) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com