
| A、C4H10、C3H6、 |
| B、C4H8、C3H8 |
| C、C4H10、C2H4 |
| D、C2H6、C3H8 |
| y |
| 4 |
| y |
| 2 |
| y |
| 4 |
| y |
| 2 |
| y |
| 4 |
| y |
| 4 |
| y |
| 4 |
| 1×(30-2-26)L |
| 2L |


科目:高中化学 来源: 题型:
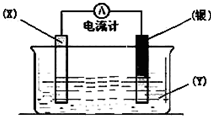 依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示.请回答下列问题:
依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| 族 周期 |
IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | |||||
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图所示,甲、乙为相互串联的两电解池.试回答:
如图所示,甲、乙为相互串联的两电解池.试回答:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加稀盐酸后过滤,除去混在铜粉中的少量镁粉和铝粉 |
| B、通入澄清石灰水,变浑浊,可说明气体中一定含二氧化碳 |
| C、用溶解、过滤的方法分离KNO3和 NaCl固体的混合物 |
| D、将氧气和氢气的混合气体通过灼热的氧化铜,以除去其中的氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、A、B、C、D |
| B、B、A、C、D |
| C、C、D、B、A |
| D、B、A、D、C |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溶液中pH由大变小 |
| B、溶液中的SO42-向原电池的正极移动 |
| C、Zn为电池的负极,电极反应:Zn-2e-═Zn2+ |
| D、在该电池的外电路导线中电子是从铜流向锌 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、当溶液中c(H+)=c(OH-)>10-7mol/L时,其pH<7,溶液呈现酸性 |
| B、室温下,pH=3的盐酸和pH=11的氨水等体积混合后,溶液中离子浓度关系是:c(Cl-)=c(NH4+)>c(OH-)=c(H+) |
| C、Na2CO3溶液中存在c(OH-)=c(HCO3-)+2c(H2CO3)+c(H+) |
| D、0.1mol/L NaHCO3中c(Na+)=c(HCO3-)+c(H2CO3)=0.1mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氧化剂和还原剂的物质的量之比为1:8 |
| B、该过程说明Fe(NO3)2不宜加酸酸化 |
| C、若有1mol NO3-发生氧化反应,则转移8mol e- |
| D、该过程说明氧化性:NO3->Fe3+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com