
【题目】常用下图所示A~D中的装置进行混合物的分离和提纯,按要求回答下列问题:

(1)仪器①的名称______________。
(2)除去Ca(OH)2溶液中悬浮的CaCO3颗粒应选用装置________(填字母代号,下同)。
(3)分离互溶的乙酸(沸点118 ℃)和乙酸乙酯(沸点77.1 ℃)的混合物应选用装置________。
(4)用CCl4提取碘水中的碘单质应选用装置________。
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】黄铜是人类最早使用的合金之一,主要由锌和铜组成。回答下列问题:
(1) 基态锌原子的核外价电子排布式为_______________,属于周期表__________区元素。电子占据最高能层的符号是_______________占据该能层电子的电子云轮廓图形状为______________
(2)第一电离能I1(Zn)________I1(Cu)(填“大于”或“小于”)
(3)向蓝色 ![]() 硫酸铜溶液中加入稍过量的氨水,溶液变为深蓝色[Cu(NH3)4] 2+。
硫酸铜溶液中加入稍过量的氨水,溶液变为深蓝色[Cu(NH3)4] 2+。
①下列微粒中与SO42-互为等电子体的是__________(填序号)。
A.H2SO4 B.CO32- C.PO43- D.CCl4
②H2O分子中心原子的杂化类型为______;NH3分子的空间构型为________。
分子中的键角:H2O_______ NH3(填“大于”或“小于”)。
③通过上述实验现象可知:与Cu2+与的配位能力H2O_________NH3 (填“大于”或“小于”)。
④极具应用前景的氨硼烷(BH3·NH3)与乙烷互为等电子体。写出BH3·NH3的结构式(结构中若含配位键用“![]() ”表示)_______________________
”表示)_______________________
(4)金属Cu晶体中的原子堆积方式如图所示,这种堆积方式称为_____________。

(5)若Cu晶体的密度为ρg/cm3,![]() 表示阿伏加德罗常数的值,列式表示Cu晶体中最近的两个Cu原子之间的距离________nm(不必化简)
表示阿伏加德罗常数的值,列式表示Cu晶体中最近的两个Cu原子之间的距离________nm(不必化简)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所涉及的物质均为中学化学中的常见物质,其中C、D、E为单质,E为固体,F为有磁性的化合物。它们之间存在如下关系(反应中生成的水及次要产物均已略去):
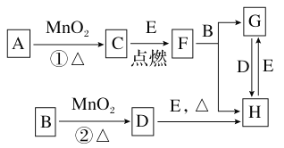
(1)写出下列物质的化学式:B________,E________。
(2)指出MnO2在相关反应中的作用:反应①中是________剂,反应②中是________剂。
(3)若反应①是在加热条件下进行,则A是________(填化学式);若反应①是在常温条件下进行,则A是________(填化学式);如在上述两种条件下得到等质量的C单质,反应中转移的电子数之比为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用甲烷与氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实。某化学兴趣小组在实验室中模拟上述过程,其设计的模拟装置如下:

试回答下列问题:
(1)请写出C装置中生成CH3Cl的化学方程式:___________________________________。有人认为E中有氯化氢产生,不能证明甲烷与氯气发生了取代反应,你认为他的看法________(填“正确”或“不正确”)。
(2)B装置有三种功能:①控制气流速率;②混匀混合气体;③________________。
(3)一段时间后发现D装置中的棉花由白色变为蓝色,则棉花上可能预先滴有________溶液。
(4)E装置中除盐酸外,还含有机物,从E中分离出盐酸的最佳方法为________(填字母)。
a.分液法 b.蒸馏法 c.结晶法
(5)将1 mol CH4与Cl2发生取代反应,充分反应后生成的CH3Cl、CH2Cl2、CHCl3、CCl4四种有机产物的物质的量依次增大0.1 mol,则参加反应的Cl2的物质的量为________,生成HCl的总物质的量为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三种气体X、Y、Z的相对分子质量关系为Mr(X)<Mr(Y)=0.5Mr(Z),下列说法正确的是
A.原子数目相等的三种气体,质量最大的是Z
B.同温同压下,同质量的三种气体,气体密度最小的是X
C.同温同压下,三种气体体积均为6.72 L,则它们的物质的量一定均为0.3 mol
D.同温下,体积相同的两容器分别充入2 g Y气体和1 g Z气体,则其压强比为2︰1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一定体积CaCl2和HCl的混合溶液中逐滴加入浓度为1 mol·L-1的Na2CO3溶液,反应过程中加入的Na2CO3溶液的体积与产生沉淀或气体的质量关系如图所示。
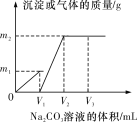
已知图中V1∶V2=1∶2;当加入V2 mL Na2CO3溶液时,所得溶液的浓度为1 mol·L-1,体积为200 mL。求:
(1)加入V2 mL Na2CO3溶液时,所得溶液的溶质是________。
(2)原混合溶液中CaCl2和HCl的物质的量之比n(CaCl2)∶n(HCl)=________。
(3)m1=________g,m2=________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出下列水溶液中的电离方程式或发生反应的离子方程式:
(1)小苏打溶于水___;
(2)用稀硫酸除掉镁条表面的氧化膜___;
(3)用胃舒平(有效成分是Al(OH) 3)治疗胃酸(主要成分是盐酸)过多___;
(4)用锌粉除去硫酸钾溶液中的Cd2+杂质(置换反应)___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某厂排出的废液主要含Zn(NO3)2和AgNO3,为了从中回收金属银和硝酸锌,某中学化学课外活动小组设计了以下的实验步骤:(已知:银可溶于硝酸;Zn(NO3)2高温下易分解,Zn(NO3)2的溶解度在溶液中受温度的影响较大)
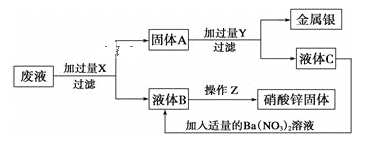
(1)X、Y分别是X:___,Y:___。(写化学式)
(2)固体A的主要成分是___。(写化学式)
(3)Z处进行的实验操作是:先过滤,将滤液___、___、过滤、洗涤、干燥。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求计算、整理化简并填空:
(1)若20g密度为ρgcm﹣3的硝酸钙溶液里含1gCa2+,则NO3-的物质的量浓度是____。
(2)现有mg某气体,它由双原子分子构成,它的摩尔质量为Mg/mol。若阿伏加德罗常数的值用NA表示,则:
①该气体所含原子总数为___个。
②该气体在标准状况下的体积为____L。
③该气体溶于1L水中(不考虑反应),形成的溶液密度为ρg/cm3,则该溶液的物质的量浓度为____molL-1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com