
化合物A(H3BNH3)是一种潜在的储氢材料,它可由六元环状物质(HB=NH)3通过反应3CH4+2(HB=NH)3+6H2O→3CO2+6H3BNH3制得。有关叙述不正确的是
A.化合物A中存在配位键
B.反应前后碳原子的杂化类型不变
C.CH4、H2O、CO2分子空间构型分别是:正四面体、V形、直线形
D.第一电离能:N>O>C>B
 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案科目:高中化学 来源:2016-2017学年黑龙江、吉林两省八校高一上学期期中化学试卷(解析版) 题型:选择题
等质量的①CH4、②H2、③HC1、④SO2四种气体,在标准状况下体积由大到小的顺序是
A.②>①>③>④ B.④>③>①>② C.③>②>④>① D.①>④>②>③
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省高一上期中化学卷(解析版) 题型:选择题
下列物质的分类合理的是
A.碱性氧化物:Na2O、CaO、Mn2O7、Na2O2
B.碱:NaOH、KOH、Ba(OH)2、Na2CO3
C.铵盐:NH4Cl、NH4NO3、(NH4)2SO4、NH3·H2O
D.氧化物:CO2、NO、SO2、H2O
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省高一上期中化学卷(解析版) 题型:选择题
下列溶液中,跟100ml0.5mol/LNaCl溶液所含的Cl-物质的量浓度相同的是( )
A.100ml0.5mol/LMgCl2溶液
B.200ml0.25mol/LCaCl2溶液
C.50ml0.51mol/LNaCl溶液
D.25mL0.5mol/LNaClO溶液
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省高二上期中化学卷(解析版) 题型:填空题
氮、磷、砷为同主族元素,回答下列问题:
(1)基态As原子的核外电子排布式为___________________。
(2)稼氮砷合金材料的太阳能电池效率达40%,Ga、N、As电负性由大至小的顺序是__________________
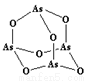
(3)As4O6的分子结构如右图所示,其中As原子的杂化方式为___________________,1 mol As4O6含有σ键的物质的量为_______________。
(4)该族氢化物RH3(NH3、PH3、AsH3)的某种性质随R的核电荷数的变化趋势如右图所示。则Y轴可表示的氢化物(RH3)性质可能是 。
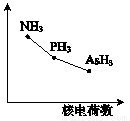
A.稳定性 | B.沸点 | C.R-H键能 | D.分子间作用力 |
(5)AsH3的沸点(-62.5℃)比NH3的沸点(-33.5℃)低,原因是
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省高二上期中化学卷(解析版) 题型:选择题
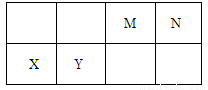
几种相邻主族短周期元素的相对位置如表,元素X的原子核外电子数是M的2倍,Y的氧化物具有两性。下列说法不正确的是
A. 元素的第一电离能X<Y
B. X位于第三周期IIA ,其单质可采用电解熔融其氯代物制备
C. 元素最高价氧化物的水化物中,酸性最强的是HNO3
D. 气体分子(MN)2的电子式为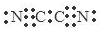
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省高二上期中化学卷(解析版) 题型:选择题
根据下表(部分短周期元素的原子半径及主要化合价)信息,以下判断不正确的是
元素代号 | A | B | C | D | E |
原子半径/nm | 0.186 | 0.143 | 0.089 | 0.102 | 0.074 |
主要化合价 | +1 | +3 | +2 | +6、-2 | -2 |
A.金属性:A>C B.氢化物的沸点H2D<H2E
C.第一电离能: A>B D.单质的熔点:A<B
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省赣州市十四校高二上学期期中化学试卷(解析版) 题型:选择题
铅蓄电池是最常见的二次电池,其构造示意图如下.发生反应的化学方程式为:Pb(s)+PbO2(s)+2H2SO4(aq) 2PbSO4(s)+2H2O(l)下列说法不正确的是( )
2PbSO4(s)+2H2O(l)下列说法不正确的是( )

A.放电时,电解质溶液的PH值 增大
增大
B.放电时,电路中转移0.2mol电子时Pb电极质量减少20.7g
C.放电时,溶液中H+向PbO2电极移动
D.放电时,正极反应为:PbO2(s)+4H+(aq)+SO42-(aq)+2e- PbSO4(s)+2H2O(l)
PbSO4(s)+2H2O(l)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林省辽源市高一上学期期中化学卷(解析版) 题型:选择题
下列微粒既有氧化性又有还原性的是
A.H+ B.Fe2+ C.Cu2+ D.Al
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com