
| A. | 若A为黄绿色气体,则D可能有漂白性 | |
| B. | 若A为红色金属单质,则D一定是红棕色气体 | |
| C. | 若A为纯碱,则D一定能使澄清石灰水变浑浊 | |
| D. | 若A为氯化铵,则D一定是具有刺激性气味的气体 |
分析 A.若A为黄绿色气体,则A为氯气,若B为NaOH,反应生成NaCl、NaClO与水,NaClO具有漂白性;
B.若A为红色金属单质,则A为Cu,B可以为浓硫酸或硝酸;
C.若A为纯碱,C属于盐类,由于反应生成水,则B为酸或酸性溶液,D为二氧化碳;
D.若A为氯化铵,C属于盐类,由于反应生成水,则B为碱,D为氨气.
解答 解:A.若A为黄绿色气体,则A为氯气,若B为NaOH,反应生成NaCl、NaClO与水,NaClO有强氧化性,具有漂白性,故A正确;
B.若A为红色金属单质,则A为Cu,B可以为浓硫酸或硝酸,Cu与浓硫酸反应生成二氧化硫,与稀硝酸反应生成NO,与浓硝酸反应生成二氧化氮,D不一定是红棕色气体,故B错误;
C.若A为纯碱,C属于盐类,由于反应生成水,则B为酸或酸性溶液,D为二氧化碳,二氧化碳能使澄清石灰水变浑浊,故C正确;
D.若A为氯化铵,C属于盐类,由于反应生成水,则B为碱,D为氨气,氨气是具有刺激性气味的气体,故D正确,
故选:B.
点评 本题考查元素化合物性质与转化,难度不大,关键是熟练掌握元素化合物性质,较好的考查学生发散思维、分析推理能力.


 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 可用电解饱和的MgCl2溶液的方法获得金属镁 | |
| B. | 电解CuSO4溶液精炼金属铜时,用铁做阳极 | |
| C. | 电解熔融Al2O3方法冶炼金属铝时,同时要加入冰晶石作助熔剂 | |
| D. | 工业上常采用活泼金属还原法冶炼金属银 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验步骤 | 实验现象 | 结论 |
| 取适量样品加热浓缩后加入试管中,再加入适量硫酸和铜片,加热. | 假设1成立 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
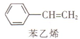
 .
.
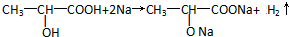 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 分类 组合 | 碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 |
| A | Na2CO3 | H2SO4 | NaHCO3 | Fe2O3 | CO2 |
| B | NaOH | NaHSO4 | NH4Cl | Na2O | NO2 |
| C | KOH | CH3COOH | NaClO | Na2O2 | SO2 |
| D | NH3•H2O | HNO3 | CaCO3 | CaO | SO3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 选项 | 离子组 | 要求 |
| A | K+、CO32-、SO42-、Cl- | c(K+)<c(Cl-) |
| B | Na+、CO32-、NO3-、I- | 滴加盐酸立刻有气体生成 |
| C | Mg2+、Cl-、Na+、SO42- | 滴加氨水立刻有沉淀生成 |
| D | NH4+、SO42-、Na+、H+ | 滴加烧碱溶液立刻有气体生成 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | A | B | C | D |
| 中心原子所在族 | ⅣA族 | ⅤA族 | ⅣA族 | ⅥA族 |
| 分子通式 | AB4 | AB3 | AB2 | AB2 |
| 立体构型 | 正四面体形 | 平面三角形 | 直线形 | V形 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+、K+、CO32-、Cl- | B. | Fe3+、K+、SCN-、NO3- | ||
| C. | Al3+、Cu2+、S2-、Cl- | D. | NH4+、Cu2+、Cl-、NO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com