
| A. | 钠保存在煤油中 | |
| B. | 用棕色试剂瓶盛放新制的氯水 | |
| C. | 冷的浓硝酸不能用钢瓶保存 | |
| D. | 向盛放氯化亚铁溶液的试剂瓶中加少量铁粉 |
分析 A.依据钠密度大于煤油,与煤油不反应,且性质活泼易于空气中氧气水反应;
B.氯水中的次氯酸见光分解;
C.依据浓硝酸的强氧化性解答;
D.二价铁离子具有强的还原性,易被空气氧化.
解答 解:A.钠保存在煤油中,可以隔绝空气,故A正确;
B.氯水中的次氯酸见光分解,所以新制氯水应用棕色瓶保存,故B正确;
C.浓硝酸具有强氧化性,常温下能够使铁钝化,所以可用钢瓶存放冷的浓硝酸,故C错误;
D.二价铁离子具有强的还原性,易被空气氧化,所以向盛放氯化亚铁溶液的试剂瓶中加少量铁粉可以防止二价铁离子被氧化变质,故D正确;
故选:C.
点评 本题考查试剂的存放,明确物质的性质与保存方法的关系是解答本题的关键,题目难度不大.


 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案科目:高中化学 来源: 题型:解答题
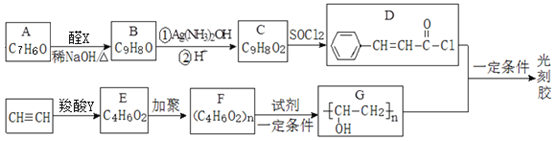
 +
+ $→_{△}^{稀NaOH}$
$→_{△}^{稀NaOH}$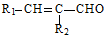 (R1,R2为烃基或氢)
(R1,R2为烃基或氢) +R2OH$\stackrel{一定条件}{→}$
+R2OH$\stackrel{一定条件}{→}$ +HCl(R1,R2为烃基)
+HCl(R1,R2为烃基) .
. .
.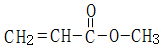
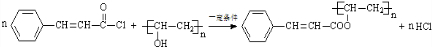 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

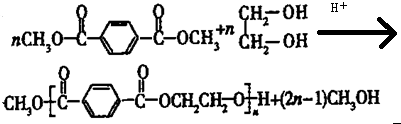 .
. 合成
合成  的流程图(注明反应条件)
的流程图(注明反应条件)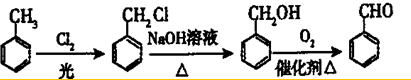 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
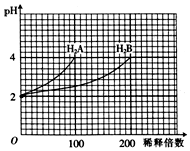 常温下,取pH=2的两种二元酸H2A和H2B各1mL,分别加水稀释,测得溶液pH与加水稀释倍数关系曲线如图所示,则下列叙述正确的是( )
常温下,取pH=2的两种二元酸H2A和H2B各1mL,分别加水稀释,测得溶液pH与加水稀释倍数关系曲线如图所示,则下列叙述正确的是( )| A. | H2A的电离方程式为H2A?H++HA-、HA-?H++A2- | |
| B. | pH=4的NaHA水溶液中:c(Na+)>c(HA-)>c(A2-)>c(H2A)>c(OH-) | |
| C. | 含NaHA、NaHB的混合溶液中,各离子浓度关系为c(Na+)=c(A2-)+c(HB-)+c(H2B)+c(B2-) | |
| D. | NaHB水溶液中,各离子浓度的大小顺序为c(Na+)>c(HB-)>c(OH-)>c(H+)>c(B2-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

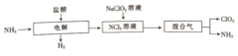
| A. | 电极b与外电源的负极相连 | |
| B. | 电解时,OH-、尿素分子均可穿过隔膜进入左室 | |
| C. | a极反应式为:CO(NH2)2-6e-+H2O═CO2↑+N2↑+6H+ | |
| D. | 每消耗1g尿素则产生标准状况下1.12LH2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纯碱用于制造玻璃 | B. | 工业上利用合成氨实现人工固氮 | ||
| C. | 打磨磁石制指南针 | D. | 医疗上用小苏打治疗胃酸过多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2 g H2的分子数为NA | |
| B. | 标准状况下,22.4 L H2O含有NA个水分子 | |
| C. | 7.8 g过氧化钠与足量水反应转移的电子数为0.2NA | |
| D. | 1 mol/L Mg(NO3)2溶液中含有NO3-的数目为2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com