
【题目】随着建筑装饰材料进入百姓家庭,某些装饰不久的居室由于装饰材料释放出来的污染物浓度过高,影响人体健康.这些污染物最常见的是( )
A.一氧化碳
B.二氧化硫
C.臭氧
D.甲醛、苯等挥发性有机物
 同步奥数系列答案
同步奥数系列答案科目:高中化学 来源: 题型:
【题目】资源的高效利用对保护环境、促进经济持续健康发展具有重要作用,如回收利用电解精炼铜的阳极泥中含有的银、铂、金等贵重金属。提炼阳极泥的方法有多种,湿法提炼是其中重要的一种,其主要生产流程如下:
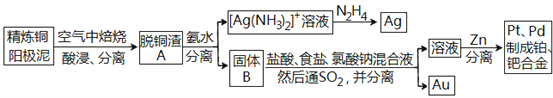
请回答下列问题:
(1)各步生产流程中都涉及了同一种分离方法,该方法需要的玻璃仪器有玻璃棒和_______。
(2)脱铜渣A中含有AgCl,它溶于浓氨水的离子方程式为________________。
(3)已知N2H4被银氨溶液氧化的产物是氮气,则每生成1molAg,需要消耗_______g N2H4。
(4)固体B中单质Au在酸性环境下与NaClO3、NaCl反应生成NaAuCl4;在NaAuCl4中Au元素的化合价为______,该反应的离子方程式为____________________。
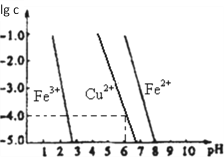
(5)阳极泥中的铜可以用FeC13溶液浸出,所得溶液主要含有的阳离子为Cu2+、Fe3+和Fe2+;结合如图分析:(其中的纵坐标代表金属阳离子浓度的对数)
①要从浸出液中提纯铜,最好先加入酸化的双氧水,目的是_______________,然后加入适量的CuO调节pH=3.7,除去______离子;
②从图中数据计算可得Cu(OH)2的Ksp约为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列操作不能用于检验NH3的是( )
A. 气体使湿润的酚酞试纸变红 B. 气体使湿润的红色石蕊试纸变蓝
C. 气体与浓硫酸靠近 D. 气体与浓盐酸靠近
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组在实验室探究二氧化氮与水的反应,实验过程如下:

实验一:制取二氧化氮
(1)在图1装置中用铜与浓硝酸反应制取并收集二氧化氮。在加入药品前,必须进行的实验操作是______________;图l装置的缺点是_______________。
实验二:二氧化氮溶于水
(2)将盛满二氧化氮的试管A倒扣入水中(如图2),轻轻晃动试管,一段时间后观察到的现象是_________________________;反应的化学方程式是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某固体可能含有NH4+、Cu2+、Na+、Cl﹣、CO32﹣、SO42﹣中的几种离子,取等质量的两份该固体,进行如下实验(不考虑盐类的水解及水的电离);
①一份固体溶于水得无色透明溶液,加入足量BaCl2溶液,得沉淀4.46g,在沉淀中加入过量稀盐酸,沉淀没变化.
②另一份固体与过量NaOH固体混合后充分加热,产生使湿润的红色石蕊试纸变蓝色的气体0.672L(保准状况).
下列说法正确的是( )
A.该固体中一定含有NH4+、SO42﹣、Na+
B.该固体中一定没有Cu2+、Cl﹣
C.该固体中只含有NH4+、CO32﹣、SO42﹣、Cl﹣
D.根据以上实验,无法确定该固体中有Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cl2与NaOH溶液反应可生成NaCl、NaClO和NaClO3(Cl﹣和ClO﹣)的比值与反应的温度有关,用40gNaOH配成的250mL溶液,与Cl2恰好完全反应(忽略Cl2与水的反应、盐类的水解及溶液体积变化):
(1)NaOH溶液的物质的量浓度molL﹣1;
(2)某温度下,反应后溶液中c(Cl﹣)=6c(ClO﹣),则溶液中c(ClO﹣)=molL﹣1 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是元素周期表的一部分,下列说法中,正确的是( )
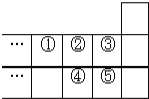
A. 元素的最高正化合价:![]()
B. 一定条件下,①和②的单质都只能形成一种氢化物
C. 38 g ③的单质跟足量水反应时,发生转移的电子为1mol
D. 元素④在自然界中存在游离态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在一个小烧杯里加入约20g已研磨成粉末的氢氧化钡晶体[Ba(OH)2·8H2O],将小烧杯放在事先已滴有3~4滴水的玻璃片上,然后,再加入约10gNH4Cl晶体,并立即用玻璃棒迅速搅拌。使Ba(OH)2·8H2O与NH4Cl充分反应。实验中观察到的现象是______________________,说明该反应是___________热反应,这是由于反应物所具有的总能量_________ (填“大于”、“小于”或“等于”生成物所具有的总能量。
(2)将Fe+2FeCl3=3FeCl2设计为一个原电池,则该电池的负极材料为__________,正极电极反应式为__________________________________。
(3)恒温下,将amo1N2与bmolH2的混合气体通入一容积固定的密闭容器中,发生如下反应:N2(g)+ 3H2(g)![]() 2NH3(g)。若反应进行到时刻t时,nt(N2)=13mol,nt(NH3)=6mol,则a=__________。反应达平衡时,混合气体的体积为716.8L(已经折算为标准状况下),其中NH3的体积分数为25%。则平衡时H2的转化率为____________________。
2NH3(g)。若反应进行到时刻t时,nt(N2)=13mol,nt(NH3)=6mol,则a=__________。反应达平衡时,混合气体的体积为716.8L(已经折算为标准状况下),其中NH3的体积分数为25%。则平衡时H2的转化率为____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com