
| A. | H2O2的氧化性比Fe3+强,其还原性比Fe2+强 | |
| B. | 在该实验中,最终溶液仍为无色 | |
| C. | 在该实验中,Fe2+和Fe3+总量保持不变 | |
| D. | H2O2值能的电子,不能失电子 |
分析 A.氧化还原反应中氧化剂的氧化性大于氧化产物,还原剂的还原性大于还原产物;
B.亚铁离子为浅绿色;
C.总反应为2H2O2═2H2O+O2↑,Fe2+为H2O2分解的催化剂,Fe2+和Fe3+的总量保持不变;
D.H2O2中O元素的化合价即升高又降低.
解答 解:A.反应2Fe2++H2O2+2H+═2Fe3++2H2O中,Fe2+被H2O2氧化生成Fe3+,故H2O2的氧化性比Fe3+强;反应中亚铁离子为还原剂,则H2O2的还原性比Fe2+弱,故A错误;
B.总反应为2H2O2═2H2O+O2↑,反应后溶液中含有亚铁离子,亚铁离子为浅绿色,故B错误;
C.总反应为2H2O2═2H2O+O2↑,Fe2+为H2O2分解的催化剂,Fe2+和Fe3+的总量保持不变,故C正确;
D.2H2O2═2H2O+O2↑,反应中H2O2中O元素的化合价即升高又降低,H2O2即得电子,又失电子,故D错误;
故选C.
点评 本题考查氧化还原反应以及化学反应的探究,题目难度中等,注意从化合价的角度分析氧化还原反应,侧重于考查学生的分析能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
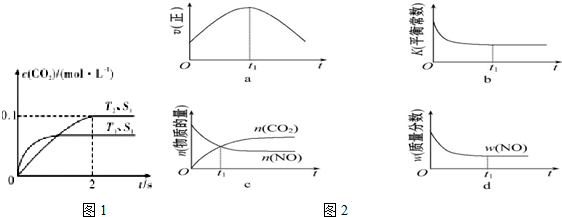
 在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该合金的熔点介于钠、铝之间 | |
| B. | 钠或铝形成的氧化物均为碱性氧化物 | |
| C. | 等质量钠和铝分别与足量的盐酸反应钠产生的气体多 | |
| D. | 若合金中n(Na)=n(Al),将其投入到足量的水中,可得无色透明溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜和稀硝酸的反应:Cu2++4H++2NO3-═Cu2++2NO2↑+2H2O | |
| B. | 氯气与水反应:Fe3++Cu═Fe2++Cu2+ | |
| C. | 氯化铝溶液加入氨水:Al3++3OH-═Al(OH)3↓ | |
| D. | 实验室制氯气:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定含有CO32- | B. | 一定含有Ag+ | ||
| C. | 一定含有SO42- | D. | 可能含有SO42-也可能含有Ag+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
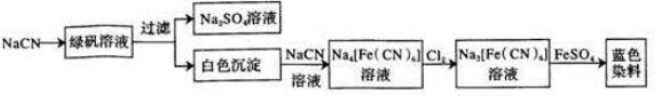
. 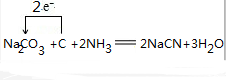 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com