
(6��)��1���ڱ�״���£����������ʣ���4 g H2 ��33.6 L CH4 ��1 mol H2O ��3.01��1023��O2 �����к������������ǣ����ں�������д��ţ���ͬ�� ����ԭ�������ٵ��� ������������ �������С���� ��
��2����0.4 mol Al3����Al2(SO4)3��������SO42һ�����ʵ����� ��
��3����1��H2O�к���a����ԭ�ӣ����ӵ������ú�a�Ĵ���ʽ�ɱ�ʾΪ ��
��1���٣��ܣ��ڣ��ۣ� ��2��0.6mol�� ��3��9a mol-1��
��������
�����������1����4gH2��n��H2��=2mol��N��H2��=2NA��N��H��=4NA��v��H2��=44.8L���ڱ�״����33.6L CH4��n��CH4��=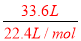 =1.5mol��N��CH4��=1.5NA��ԭ������Ϊ5��1.5NA=7.5NA������Ϊm��CH4��=1.5mol��16g/mol=24g����1molH2O�ķ�����ΪN��H2O��=1NA��ԭ������Ϊ3NA�����ԼΪ18ml������Ϊ1mol��18g/mol=18g����3.01��1023��O2�����ʵ���Ϊn��O2��=0.5mol��ԭ������Ϊ1NA�����Ϊ11.2L������Ϊ0.5mol��32g/mol=16g�����Ϸ�����֪���������������Ǣ٣���ԭ�������ٵ��Ǣܣ����������Ǣڣ������С�Ģۣ��ʴ�Ϊ�٣��ܣ��ڣ��ۣ���2��Al2��SO4��3��n��Al3+����n��SO42-��=2��3��n��Al3+��=0.4mol����n��SO42-��=0.6mol����3��1gˮ�����ʵ���Ϊ��n��H2O��=
=1.5mol��N��CH4��=1.5NA��ԭ������Ϊ5��1.5NA=7.5NA������Ϊm��CH4��=1.5mol��16g/mol=24g����1molH2O�ķ�����ΪN��H2O��=1NA��ԭ������Ϊ3NA�����ԼΪ18ml������Ϊ1mol��18g/mol=18g����3.01��1023��O2�����ʵ���Ϊn��O2��=0.5mol��ԭ������Ϊ1NA�����Ϊ11.2L������Ϊ0.5mol��32g/mol=16g�����Ϸ�����֪���������������Ǣ٣���ԭ�������ٵ��Ǣܣ����������Ǣڣ������С�Ģۣ��ʴ�Ϊ�٣��ܣ��ڣ��ۣ���2��Al2��SO4��3��n��Al3+����n��SO42-��=2��3��n��Al3+��=0.4mol����n��SO42-��=0.6mol����3��1gˮ�����ʵ���Ϊ��n��H2O��=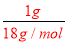 =
=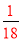 mol��
mol��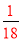 molˮ�к���Hԭ�ӵ���Ŀ=
molˮ�к���Hԭ�ӵ���Ŀ=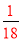 mol��2NA=a����٤������NA=
mol��2NA=a����٤������NA=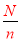 =
=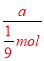 ==9amol-1��
==9amol-1��
���㣺���ʵ����ļ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��SO2��NO��CO2���ᵼ��������γ� | B���ȱȹ衢���ά���������մɵ������������ǽ������� | C����ȩ�ĺ�������ʳƷ��ȫ����ָ�� | D��Һ�ȹ�й©ʱ���ɽ�������ˮ���в�������ʯ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015��㶫ʡ�ع���ʮУ����10��������ѧ�Ծ��������棩 ���ͣ�ѡ����
��һ��iPhone���ڵ�ط��������Ľ����õ�ص�һ��Ϊһ���л��߷��������(��R��ʾ)��ʯī�ۼ�ճ����ĸ������һ����ﮣ��ָ�����Ϊij�־�ϩ���������ΪLiPF6�ܽ���ij���л�̼�����ܼ��С��������(R)�ڿ�����ʮ���ȶ����ڳ��ʱ��������������(Rx+)����س�ŵ�ķ���ʽΪ��xLi��Rx+ xLi����R�������й�˵����ȷ���ǣ� ��
xLi����R�������й�˵����ȷ���ǣ� ��
A���ŵ�ʱ���õ�ؽ�����ת��Ϊ��ѧ��
B�����ʱ��Rx+�������������ƶ�
C���ŵ�ʱ��������ӦΪxLi��xe����xLi��
D�����ʱ��������ӦΪR��xe����Rx+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015��㶫ʡտ���и�����һ���¿����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����£����и���������ָ����Һ��һ���ܴ����������( )
A��0��1 mol��L��1 NaOH��Һ��K����Ba2+��Cl����HCO3-
B��0��1 mol��L��1 Na2CO3��Һ��K����NH ��NO
��NO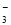 ��SO
��SO
C��0��1 mol��L��1 FeCl3��Һ��K����Na����I����SCN��
D��0��1 mol��L��1 HCl����Һ��Ca2����Na����ClO����NO
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015��㶫ʡտ���и�һ��һѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���������ҹ������Ļ�ѧ�ң�1991����ȷ���In�����ԭ������Ϊ114.818�����������ԭ������ίԱ�����Ϊ�µı�ֵ���������ԭ�����������״β����ҹ��ⶨ�����ԭ������ֵ�������й��ڵ�˵���У��������
A�� Inԭ�Ӻ�����49������
Inԭ�Ӻ�����49������
B�� Inԭ�Ӻ�����49������
Inԭ�Ӻ�����49������
C�� Inԭ�Ӻ�����������������֮�͵�����������Ϊ115
Inԭ�Ӻ�����������������֮�͵�����������Ϊ115
D�� In��InԪ�ص�һ�ֺ���
In��InԪ�ص�һ�ֺ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ�γ��С��������и�һ��ѧ������������ѧ�Ծ��������棩 ���ͣ�ѡ����
����NaCl����ѷ�����
A����ɫ��Ӧ�ʻ�ɫ���������ữ��AgNO3��Һ�а�ɫ����
B����ɫ��Ӧ����ɫ���������ữ��AgNO3��Һ�а�ɫ����
C����ɫ��Ӧ�ʻ�ɫ���������ữ��AgNO3��Һ�а�ɫ����
D����ɫ��Ӧ����ɫ���������ữ��AgNO3��Һ�а�ɫ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ�γ��С��������и�һ��ѧ������������ѧ�Ծ��������棩 ���ͣ�ѡ����
����ͬ�����£����и��������У�������һ����ͬ����
A��34g NH3��4g H2 B��14g N2��32g O2
C��2L CO2��2L H2O D��11.2L O2��0.5mol H2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ�����и�����ѧ�ڵ�һ�ν��Բ��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����й���Һ����Ũ�ȹ�ϵ��������ȷ����
A��0.1 mol��L��1NH4Cl��Һ�У�c��NH4����>c��Cl����>c��H����>c��OH����
B�����е����ʵ���NaClO��NaHCO3����Һ�У�c(HClO)��c(ClO��)��c(HCO3��)��c(H2CO3)��c(CO32��)
C��pH��5.6��CH3COOH��CH3COONa�����Һ�У�c(Na+)��c(CH3COO��)
D��25��ʱ��pH=7��NH4Cl��NH3��H2O�����Һ��c(H+)= c(OH��)=c(NH4��)=c(Cl��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ̩���н������߶���ѧ���п��Ի�ѧ�Ծ���ѡ�ޣ��������棩 ���ͣ�ѡ����
��300 mL���ܱ������У��������۲�����һ������CO���壬һ�������·�����Ӧ��
Ni(s)��4CO(g)  Ni(CO)4(g)����֪�÷�Ӧƽ�ⳣ�����¶ȵĹ�ϵ���±�������˵����ȷ����
Ni(CO)4(g)����֪�÷�Ӧƽ�ⳣ�����¶ȵĹ�ϵ���±�������˵����ȷ����
�¶�/�� | 25 | 80 | 230 |
ƽ�ⳣ�� | 5��104 | 2 | 1.9��10��5 |
A����������Ni(CO)4�ķ�ӦΪ���ȷ�Ӧ
B��25 ��ʱ����ӦNi(CO)4(g)  Ni(s)��4CO(g)��ƽ�ⳣ��Ϊ2��10��5
Ni(s)��4CO(g)��ƽ�ⳣ��Ϊ2��10��5
C��80 ��ﵽƽ��ʱ�����n(CO)��0.3 mol����Ni(CO)4��ƽ��Ũ��Ϊ2 mol��L��1
D��80 ��ʱ�����ijʱ��Ni(CO)4��CO��Ũ�Ⱦ�Ϊ0.5 mol��L��1�����ʱ��(��)���ԣ���)
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com