
| A. | 标准状况时11.2LO2的质量为32g | B. | 16O的相对原子质量为32 | ||
| C. | 44gCO2和28gCO含有相同的分子数 | D. | 标准状况时44gCO2的体积是22.4L |
分析 假设12C的相对原子质量为24,但碳的摩尔质量不变,则其它物质的摩尔质量、标况下的气体摩尔体积都不发生变化,根据n=$\frac{m}{M}$=$\frac{V}{{V}_{m}}$=$\frac{N}{{N}_{A}}$计算.
解答 解:阿伏伽德罗常数没有变化,则各物质的摩尔质量、气体摩尔体积不变,
A.标准状况下11.2L氧气的物质的量为0.5mol,氧气的质量为:32g/mol×0.5mol=16g,故A错误;
B.氧原子的实际质量没变,但标准却由12C质量的$\frac{1}{12}$变为$\frac{1}{24}$,所以氧原子的相对原子质量由16变为32,故B正确;
C.44g二氧化碳的物质的量n=$\frac{44g}{44g/mol}$=1mol,分子数为NA,28gCO的物质的量n=$\frac{28g}{28g/mol}$=1mol,分子数为NA,二者含有的分子数相同,故C正确;
D.44g二氧化碳的物质的量n=$\frac{44g}{44g/mol}$=1mol,在标准状况下的体积V=1mol×22.4L/mol=22.4L,故D正确;
故选A.
点评 本题考查物质的量的计算,题目难度中等,标准由12C质量的$\frac{1}{12}$变为$\frac{1}{24}$后,各原子的相对原子质量或摩尔质量加倍是解题的关键.


科目:高中化学 来源: 题型:选择题
| A. | 凡需加热的反应一定是吸热反应 | |
| B. | 反应物的总能量比生成物的总能量大 | |
| C. | 氢氧化钠与盐酸的反应属于吸热反应 | |
| D. | CO2与CaO化合是放热反应,则CaCO3分解是吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
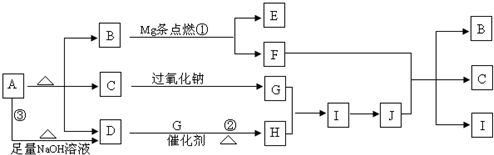
 ,C是极性(极性、非极性)分子,D分子的空间构型为三角锥形.
,C是极性(极性、非极性)分子,D分子的空间构型为三角锥形.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 混合气体一定是CH4和C2H4 | |
| B. | 混合气体中一定有CH4,可能含有C2H4 | |
| C. | 混合气体中一定含有CH4,可能含有C2H6 | |
| D. | 混合气体中可能含有C2H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | 结构或性质信息 |
| T | 原子的L层上s电子数等于p 电子数 |
| X | 元素的原子半径是第三周期主族元素中最大的 |
| Y | 空气中含其单质,原子的最外层未成对电子数是该元素所在周期中最多的 |
| Z | 单质常温、常压下是气体.原子的M层上有1个未成对的p电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
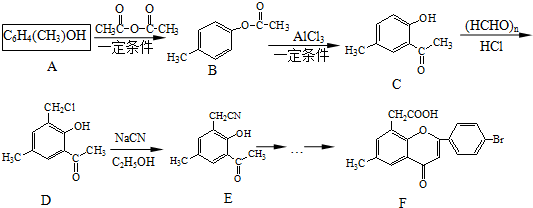
 .
.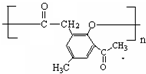 .
.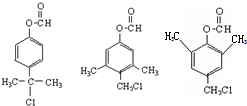 .
.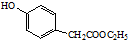 )是一种重要的医药中间体.完成以A和乙醇为主要原料制备对羟基苯乙酸乙酯的合成路线流程图(无机试剂任选).
)是一种重要的医药中间体.完成以A和乙醇为主要原料制备对羟基苯乙酸乙酯的合成路线流程图(无机试剂任选). $→_{一定条件}^{Cl_{2}}$
$→_{一定条件}^{Cl_{2}}$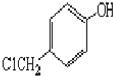
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol H2SO4的质量为98g•mol-1 | |
| B. | H2SO4的摩尔质量为98g | |
| C. | 6.02×1022个H2SO4分子的质量为9.8g | |
| D. | 9.8 g H2SO4含有6.02×1023个H2SO4分子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com