
| A. | H2SO4 | B. | Na2O2 | C. | Fe(OH)3 | D. | AlCl3 |
分析 A、三氧化硫与水反应生成硫酸,没有元素化合价的变化属于非氧化还原反应,亚硫酸与氧气反应生成硫酸,属于氧化还原反应;
B、Na与氧气加热反应生成过氧化钠,属于氧化还原反应;
C、氢氧化亚铁、氧气以及水之间反应生成氢氧化铁,属于氧化还原反应;
D、铝与氯气反应生成AlCl3,属于氧化还原反应.
解答 解:A、三氧化硫与水反应生成硫酸,属于化合反应,反应中没有元素化合价的变化属于非氧化还原反应,亚硫酸与氧气反应生成硫酸属于化合反应,反应中S、O元素的化合价发生变化,属于氧化还原反应,故A正确;
B、Na与氧气加热反应生成过氧化钠,属于氧化还原反应,该物质只能通过氧化还原反应生成,故B错误;
C、氢氧化亚铁、氧气以及水之间反应生成氢氧化铁,属于氧化还原反应,该物质只能通过氧化还原反应生成,故C错误;
D、铝与氯气反应生成AlCl3,属于氧化还原反应,该物质只能通过氧化还原反应生成,故D错误.
故选A.
点评 本题考查了氧化还原反应、物质间的反应,明确物质的性质是解本题关键,根据物质的性质来分析解答,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | pH=2的HA溶液与pH=12的MOH溶液任意比混合:c(H+)+c(M+)═c(OH-)+c(A-) | |
| B. | pH相等的CH3COONa、NaOH和Na2CO3三种溶液:c(NaOH)<c(CH3COONa)<c(Na2CO3) | |
| C. | 物质的量浓度相等CH3COOH和CH3COONa溶液等体积混合:c(CH3COO-)+2c(OH-)═c(H+)+c(CH3COOH) | |
| D. | 0.1mol•L-1的NaHA溶液,其pH=4:c(HA-)>c(H+)>c(H2A)>c(A2-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
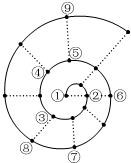 如果将前18号元素按原子序数递增的顺序排列,可形成图所示的“蜗牛”形状,图中每个“•”代表一种元素,其中①点代表氢元素.下列有关说法正确的是( )
如果将前18号元素按原子序数递增的顺序排列,可形成图所示的“蜗牛”形状,图中每个“•”代表一种元素,其中①点代表氢元素.下列有关说法正确的是( )| A. | 最简单气态氢化物的稳定性:③比⑧强、⑤比⑨弱 | |
| B. | 最高价氧化物对应水化物的碱性:②比⑥强 | |
| C. | ⑦的最高价氧化物对应的水化物具有两性 | |
| D. | 简单离子半径④比⑥小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(H+)=c(CH3COO-) | |
| B. | 溶液中:c(H+)>c(OH-) | |
| C. | CH3COOH分子的浓度不再变化 | |
| D. | 溶液中同时存在H+、CH3COO-、OH-、CH3COOH、H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 金属镁在目前的汽车、航天、航空、机械制造、军事等产业中得判迅猛发展.
金属镁在目前的汽车、航天、航空、机械制造、军事等产业中得判迅猛发展.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子数之比为1:1 | B. | 原子数之比为1:1 | C. | 中子数之比为1:1 | D. | 密度之比为1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO的燃烧热为566.0 kJ•mol-1 | |
| B. | 2 mol CO和1 mol O2的总能量比2 mol CO2的总能量低 | |
| C. | 完全燃烧20g甲醇,生成二氧化碳和液态水时放出的热量为908.3 kJ | |
| D. | 2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)a=-1453.28 kJ•mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com