
 (1)C中存在的化学键类型为______;G的电子式为______.
(1)C中存在的化学键类型为______;G的电子式为______.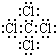 ,故答案为:离子键、共价键;
,故答案为:离子键、共价键;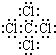 ;
; 4Al+3O2↑,
4Al+3O2↑, 4Al+3O2↑;
4Al+3O2↑;

 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
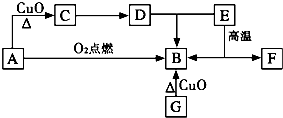 A是生活中最常见的有机物,该化合物的蒸气对氢气的相对密度是23,是生物燃料之一.C的溶液能发生银镜反应,反应后的溶液经酸化可得D.G为单质,其原子最外层电子数为次外层的2倍.F中阴阳离子个数比为1:1,其阳离子与Ar具有相同的电子层结构,A-F的转化关系如图.?
A是生活中最常见的有机物,该化合物的蒸气对氢气的相对密度是23,是生物燃料之一.C的溶液能发生银镜反应,反应后的溶液经酸化可得D.G为单质,其原子最外层电子数为次外层的2倍.F中阴阳离子个数比为1:1,其阳离子与Ar具有相同的电子层结构,A-F的转化关系如图.?查看答案和解析>>
科目:高中化学 来源: 题型:
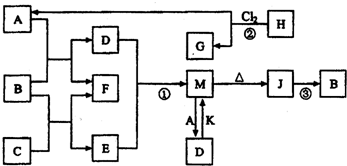
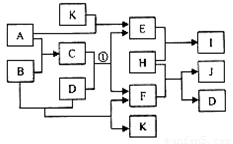
(4分)图中各物质均由常见元素(原子序数≤20)组成。已知A、B、K为单质,且在常温下A和K为气体,B为固体。D为常见的无色液体。I是一种常用的化肥,在其水溶液中滴加AgNO3溶液有不溶于稀HNO3的白色沉淀产生。J是一种实验室常用的干燥剂。它们的相互转化关系如图所示(图中反应条件未列出)。
请回答下列问题:
(1)I的化学式为 (1分); J的电子式为 (1分)
(2)F的水溶液与氯气反应的离子方程式为 (2分)
查看答案和解析>>
科目:高中化学 来源:2010年江西省高三10月月考化学试题 题型:填空题
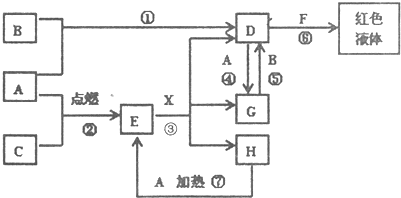
(10分)如图A~J均代表无机物或其水溶液,其中B、D、G是单质,B是地壳中含量最高的金属元素,G是气体,J是磁性材料,常温下H为无色液体。图中B和C的水溶液反应生成F和G。

根据图示回答问题:
(1)写出E的化学式: E___ ,H的电子式H_____;
(2)反应①的离子方程式是_________________;
反应②的化学方程式是_____________________;
(3)J与盐酸反应的化学方程式是_______________;
反应后的溶液与D反应的离子方程式是___________________。
查看答案和解析>>
科目:高中化学 来源:2011届浙江宁海县正学中学高三上学期第一次阶段性测试化学试卷 题型:填空题
(4分)图中各物质均由常见元素(原子序数≤20)组成。已知A、B、K为单质,且在常温下A和K为气体,B为固体。D为常见的无色液体。I是一种常用的化肥,在其水溶液中滴加AgNO3溶液有不溶于稀HNO3的白色沉淀产生。J是一种实验室常用的干燥剂。它们的相互转化关系如图所示(图中反应条件未列出)。
请回答下列问题:
(1)I的化学式为 (1分); J的电子式为 (1分)
(2)F的水溶液与氯气反应的离子方程式为 (2分)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com