
| 组合编号 | A的分子式 | B的分子式 | A和B的体积比(VA:VB) |
| ① | |||
| ② | |||
| ③ | |||
| ④ |
分析 (1)根据1L碳原子数为n的烷烃或烯烃充分燃烧后均得到n升CO2,由题意(1L混合气体充分燃烧后生成2.5升CO2,且B分子的碳原子数比A分子的多)可推断,混合气体只能由碳原子数小于2.5的烷烃(CH4和C2H6)和碳原子数大于2.5的烯烃(C3H6和C4H8)组成,它们有四种可能的组合,根据每一种组合中烷烃和烯烃的碳原子数及燃烧后生成的CO2体积,利用十字交叉法可确定A和B的体积比;
(2)根据燃烧方程式利用差量法来计算.
解答 解:(1)因1升混合气体充分燃烧后生成2.5升CO2,且B分子的碳原子数比A分子的多,混合气体只能由碳原子数小于2.5的烷烃(CH4和C2H6)和碳原子数大于2.5的烯烃(C3H6和C4H8)组成.它们有四种可能的组合:CH4、C3H6;CH4、C4H8;
C2H6、C3H6;C2H6、C4H8;根据每一种组合中烷烃和烯烃的碳原子数及燃烧后生成的CO2体积,可确定A和B的体积比.如: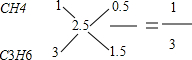 ,即V(CH4):V(C3H6)=1:3,
,即V(CH4):V(C3H6)=1:3,
所以①CH4、C3H6、1:3;②CH4、C4H8、1:1③C2H6、C3H6、1:1④C2H6、C4H8、3:1;
故答案为:
| 组合编号 | A的分子式 | B的分子式 | A和B的体积比(VA:VB) |
| ① | CH4 | C3H6 | 1:3 |
| ② | CH4 | C4H8 | 1:1 |
| ③ | C2H6 | C3H6 | 1:1 |
| ④ | C2H6 | C4H8 | 3:1 |
点评 本题主要考查了十字交叉法、差量法的使用,有一定的难度,注意根据燃烧的方程式进行判断,侧重于考查学生的分析能力和计算能力.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba(OH)2的电离方程式为:Ba(OH)2?Ba2++(OH)22- | |
| B. | 易溶于水的物质一定是电解质,难溶于水的物质一定不是电解质 | |
| C. | 硫酸铝熔化时发生了电离,可表示为:Al2(SO4)═2Al3++3SO42- | |
| D. | 虽然CO2水溶液的导电能力较弱,但CO2仍是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | n=4 | |
| B. | X的转化率为60% | |
| C. | X的平衡浓度为0.4mol/L | |
| D. | 2 min内Y的平均速率为0.4mol/(L.min) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子数 | B. | 密度 | C. | 质量 | D. | 分子数 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 制备Al(OH)3悬浊液:向1mol•L-1AlCl3溶液中加过量的6mol•L-1NaOH溶液 | |
| B. | 提纯含有少量乙酸的乙酸乙酯:向含有少量乙酸的乙酸乙酯中加入过量饱和氢氧化钠溶液,振荡后静置分液,并除去有机相的水 | |
| C. | 检验溶液中是否含有Fe2+:取少量待检验溶液,向其中滴加KSCN溶液,再加入少量新制氯水,观察实验现象 | |
| D. | 探究催化剂对H2O2分解速率的影响:在相同条件下,向一支试管中加入2mL5%H2O2和1mLH2O,向另一支试管中加入2mL5%H2O2和1mLFeCl3溶液,观察并比较实验现象 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com