
| 0.4mol |
| 5 |


 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、等于2V mL |
| B、小于2V mL |
| C、大于2V mL |
| D、无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
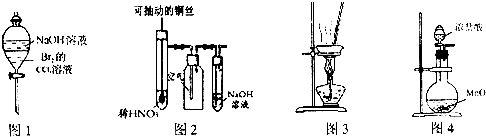
| A、图1装置可以用于除去溶解在CCl4中的Br2 |
| B、图2所示装置微热稀HNO3,在广口瓶中可收集NO气体 |
| C、用图3装置在蒸发皿中灼烧CuSO4?5H2O晶体以除去结晶水 |
| D、实验室常用图4装置制取少量氯气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
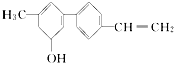 某有机化合物的结构简式如图所示:关于该化合物的下列说法正确的是( )
某有机化合物的结构简式如图所示:关于该化合物的下列说法正确的是( )| A、该有机物分子式C15H14 |
| B、完全燃烧时只有二氧化碳和水两种产物 |
| C、分子中苯环上连有羟基属于酚 |
| D、由于含有氧元素不是有机物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
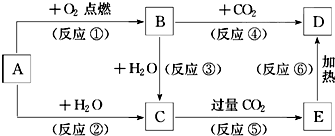 下列图示中,A为一种常见的单质,B、C、D、E是含A元素的常见化合物,它们的焰色反应均为黄色.
下列图示中,A为一种常见的单质,B、C、D、E是含A元素的常见化合物,它们的焰色反应均为黄色.查看答案和解析>>
科目:高中化学 来源: 题型:
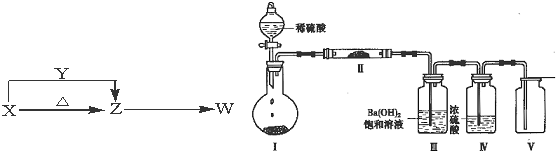
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com