
| A. | 用加热法测定胆矾晶体中结晶水含量时,若在空气中冷却会使结果偏低 | |
| B. | 配制氯化铁溶液时,先将氯化铁溶于较浓盐酸,再用蒸馏水稀释并加入少量铁粉 | |
| C. | 将甲烷和乙烯的混合气体通过盛有浓溴水的洗气瓶,即可提纯甲烷 | |
| D. | 将蔗糖和稀硫酸混合加热后,再加入银氨溶液并水浴加热,以检验还原性糖 |
分析 A.用加热法测定胆矾晶体中结晶水含量时,若在空气中冷却会导致无水硫酸铜吸收空气中的水重新形成结晶水合物,导致结果偏低;
B.配制氯化铁溶液时,先将氯化铁溶于较浓盐酸,再用蒸馏水稀释,目的是防止Fe3+水解,但不能加入铁粉,会反应生成Fe2+;
C.浓溴水中单质溴易挥发;
D.银镜反应应在碱性条件下进行.
解答 解:A.用加热法测定胆矾晶体中结晶水含量时,若在空气中冷却会导致无水硫酸铜吸收空气中的水重新形成结晶水合物,导致结果偏低;应该放在干燥器中冷却,因为在干燥器的底部放有干燥剂,不让水分进入,故A正确;
B.配制氯化铁溶液时,先将氯化铁溶于较浓盐酸,再用蒸馏水稀释,目的是防止Fe3+水解,但不能加入铁粉,会反应生成Fe2+,发生反应:2Fe3++Fe═3Fe2+,导致氯化铁变质,故B错误;
C.浓溴水中单质溴易挥发,将甲烷和乙烯的混合气体通过盛有浓溴水的洗气瓶,乙烯被吸收,得到的甲烷中会混有溴蒸气,故C错误;
D.蔗糖在酸性条件下水解生成葡萄糖,而葡萄糖发生银镜反应应在碱性条件下进行,题目没有调节溶液pH,故D错误.
故选A.
点评 本题考查常见化学实验操作、实验方案设计与评价,注意物质的化学性质和实验基本操作,难度不大,侧重于考查学生的分析能力和实验探究能力.


科目:高中化学 来源: 题型:选择题
| A. | NH3•H2O溶液的c(OH-)>NaOH溶液的c(OH-) | |
| B. | c(Na+)=c(NH4+) | |
| C. | 等体积的氢氧化钠和氨水溶液分别与足量盐酸完全反应,NaOH消耗的盐酸体积多 | |
| D. | 将pH值相等的氢氧化钠和氨水溶液加水稀释相同倍数,氨水溶液的pH大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④⑤ | B. | ①②⑤ | C. | ①②④ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 如下图的转化关系中,已知A是由短周期元素组成的酸式盐.D、Y、H为气体,X为无色液体,G和K均是常见的强酸.H与Na2O2可发生化合反应,生成的盐与Ba2+反应可生成不溶于稀G的白色沉淀,一个D分子中含有10个电子.
如下图的转化关系中,已知A是由短周期元素组成的酸式盐.D、Y、H为气体,X为无色液体,G和K均是常见的强酸.H与Na2O2可发生化合反应,生成的盐与Ba2+反应可生成不溶于稀G的白色沉淀,一个D分子中含有10个电子. ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
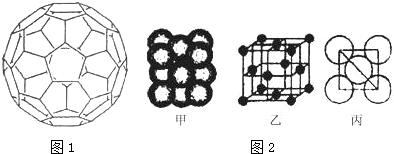
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
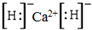 ;这种离子化合物可与水反应,化学方程式为CaH2+2H2O=Ca(OH)2+2H2↑.
;这种离子化合物可与水反应,化学方程式为CaH2+2H2O=Ca(OH)2+2H2↑.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
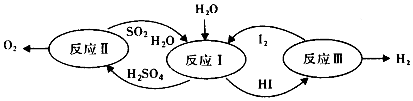
| A. | 设计该循环是为了制取能源气体O2 | |
| B. | 整个循环过程中产生1mol O2的同时产生1molH2 | |
| C. | 图中反应Ⅰ、Ⅱ、Ⅲ均可在常温常压下进行 | |
| D. | 图中反应Ⅰ、Ⅱ、Ⅲ均为氧化还原反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com