
 .
. 分析 A、B、C、D 4种短周期元素,原子序数依次增大.A、C同主族,二者可形成两种常见的化合物,其中一种是常见的严重的大气污染物,则A为O元素、C为S元素;B、C、D同周期,即处于第三周期,B的最外层电子数比其最内层电子数少1,则B为Na,结合原子序数可知D为Cl,据此解答.
解答 解:A、B、C、D 4种短周期元素,原子序数依次增大.A、C同主族,二者可形成两种常见的化合物,其中一种是常见的严重的大气污染物,则A为O元素、C为S元素;B、C、D同周期,即处于第三周期,B的最外层电子数比其最内层电子数少1,则B为Na,结合原子序数可知D为Cl.
(1)B和D形成的化合物是NaCl,由钠离子与氯离子构成,其电子式为: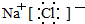 ,
,
故答案为: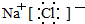 ;
;
(2)实验室利用二氧化锰与浓盐酸在加热条件下制备氯气,反应化学方程式为MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,
故答案为:MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;
(3)ICl的化学性质跟Cl2相似,化合物中I表现正极,Cl元素表现负价,故化合物ICl与水反应生成HIO与HCl,反应化学方程式为:ICl+H2O=HIO+HCl,
故答案为:ICl+H2O=HIO+HCl;
(4)因为Na2O2有强氧化性,可以用作漂白剂,因为Na2O2与CO2反应生成氧气,可以用作供氧剂,
故答案为:漂白剂、供氧剂等.
点评 本题考查位置结构性质关系应用,推断元素是解题关键,侧重对基础知识的巩固与迁移运用考查,(3)中注意根据ICl中元素化合价判断产物.


 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:多选题
| A. | 1,3-丁二烯的1,2-加成:H2C=CHCH=CH2+Cl2→CH2ClCH=CHCH2Cl | |
| B. | 甲苯和氯气光照条件下发生反应: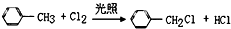 | |
| C. | 用醋酸去除水垢:CaCO3+2H+=Ca2++CO2↑+H2O | |
| D. | 用银氨溶液检验乙醛的醛基:CH3CHO+2Ag(NH4)2OH$\stackrel{水浴加热}{→}$CH3COONH4+3NH3+2Ag↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径逐渐减小 | B. | 最外层电子数逐渐增多 | ||
| C. | 最高正化合价逐渐增大 | D. | 元素的非金属性逐渐增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 阿伏加德罗、汤姆生 | B. | 道尔顿、拉瓦锡 | ||
| C. | 舍勒、普利斯特里 | D. | 汤姆生、道尔顿 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 产物中只有四氯化碳分子是正四面体结构 | |
| B. | 瓶中气体的黄绿色逐渐变浅,瓶内壁有油状液滴形成 | |
| C. | 若日光直射,可能发生爆炸 | |
| D. | 生成物只有CCl4、HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2 和D2 互为同位素 | |
| B. | 40Ca和40K中质子数和中子数都不相等 | |
| C. | 只含一种元素的物质一定是纯净物 | |
| D. | 18O中中子数和质子数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可以用NaOH溶液鉴别MgCl2和AlCl3 | |
| B. | 可以用溴水鉴别甲烷和乙烯 | |
| C. | 可以用分液漏斗分离乙酸和乙醇 | |
| D. | 可以用NaOH溶液除去苯中少量的Br2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铪-185的原子核内有72个电子 | B. | 其中子数比电子数多41 | ||
| C. | 是铪-180的一种新的同素异形体 | D. | 铪-185的原子核内有185个质子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com