
½šŹōīŃ(Ti)ŠŌÄÜÓÅŌ½£¬±»³ĘĪŖ¼ĢĢś”¢ĀĮÖ®ŗóµÄ”°µŚČż½šŹō”±”£¹¤ŅµÉĻŅŌ½šŗģŹÆĪŖŌĮĻÖĘČ”TiµÄ·“Ó¦ ĪŖ
ĪŖ
aTiO2£«bCl2£«cC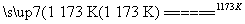 aTiCl4£«cCO””¢ń
aTiCl4£«cCO””¢ń
TiCl4£«2Mg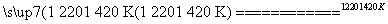 Ti£«2MgCl2””¢ņ
Ti£«2MgCl2””¢ņ
¹ŲÓŚ·“Ó¦¢ń”¢¢ņµÄ·ÖĪö²» ÕżČ·µÄŹĒ (””””)”£
ÕżČ·µÄŹĒ (””””)”£
¢ŁTiCl4ŌŚ·“Ó¦¢ńÖŠŹĒ»¹Ō²śĪļ£¬ŌŚ·“Ó¦¢ņÖŠŹĒŃõ»Æ¼Į£»¢ŚC”¢MgŌŚĮ½øö·“Ó¦ÖŠ¾łĪŖ»¹Ō¼Į£¬±»»¹Ō£»
¢ŪŌŚ·“Ó¦¢ń”¢¢ņÖŠMgµÄ»¹ŌŠŌ“óÓŚCµÄ£¬CµÄ»¹ŌŠŌ“óÓŚTiCl4µÄ£»¢Üa£½1£¬b£½c£½2£»¢ŻĆæÉś³É19.2 g Ti£¬·“Ó¦¢ń”¢¢ņÖŠ¹²×ŖŅĘ 4.8 mol e£”£
4.8 mol e£”£
A£®¢Ł¢Ś¢Ü B£®¢Ś¢Ū¢Ü C£®¢Ū¢Ü D£®¢Ś¢Ū¢Ż
½āĪö””·“Ó¦ ¢ńÖŠ£¬Cl“Ó0¼Ū½µµ½£1¼Ū£¬Ćæ·“Ó¦1 mol Cl2×ŖŅĘ2 mol e££¬C“Ó0¼ŪÉżµ½£«2¼Ū£¬Ćæ·“Ó¦1 mol C×ŖŅĘ2 mol e££¬ÅäĘ½»Æѧ·½³ĢŹ½ÓŠa£½1£¬b£½c£½2£¬¢ÜÕżČ·£»øł¾Ż»ÆŗĻ¼ŪµÄ±ä»ÆĒéæö£¬TiCl4ŌŚ·“Ó¦¢ńÖŠŹĒ»¹Ō²śĪļ£¬ŌŚ·“Ó¦¢ņÖŠŹĒŃõ»Æ¼Į£¬¢ŁÕżČ·£»»¹Ō¼Į±»Ńõ»Æ£¬¢Ś“ķĪó£»ŌŚĶ¬Ņ»·“Ó¦ÖŠ£¬»¹Ō¼ĮµÄ»¹ŌŠŌ×īĒ棬µ«MgŗĶC²»ŌŚĶ¬Ņ»·“Ó¦ÖŠ£¬ĪŽ·ØÅŠ¶ĻĘ仹ŌŠŌĻą¶Ō“󊔣¬¢Ū“ķĪó£»·“Ó¦¢ņÖŠ£¬TiÓÉ£«4¼Ū½µµ½0¼Ū£¬ĆæÉś³É1 mol Ti(¼“48 g)×ŖŅĘ4 mol e££¬¹ŹĆæÉś³É19.2 g Ti(¼“0.4 mol)×ŖŅĘ1.6 mol e££¬½įŗĻ·“Ó¦¢ńĆæÉś³É0.4 mol TiCl4×ŖŅĘ1.6 mol e££¬·“Ó¦¢ń”¢¢ņÖŠ¹²×ŖŅĘ3.2 mol e££¬¢Ż“ķĪó”£
¢ńÖŠ£¬Cl“Ó0¼Ū½µµ½£1¼Ū£¬Ćæ·“Ó¦1 mol Cl2×ŖŅĘ2 mol e££¬C“Ó0¼ŪÉżµ½£«2¼Ū£¬Ćæ·“Ó¦1 mol C×ŖŅĘ2 mol e££¬ÅäĘ½»Æѧ·½³ĢŹ½ÓŠa£½1£¬b£½c£½2£¬¢ÜÕżČ·£»øł¾Ż»ÆŗĻ¼ŪµÄ±ä»ÆĒéæö£¬TiCl4ŌŚ·“Ó¦¢ńÖŠŹĒ»¹Ō²śĪļ£¬ŌŚ·“Ó¦¢ņÖŠŹĒŃõ»Æ¼Į£¬¢ŁÕżČ·£»»¹Ō¼Į±»Ńõ»Æ£¬¢Ś“ķĪó£»ŌŚĶ¬Ņ»·“Ó¦ÖŠ£¬»¹Ō¼ĮµÄ»¹ŌŠŌ×īĒ棬µ«MgŗĶC²»ŌŚĶ¬Ņ»·“Ó¦ÖŠ£¬ĪŽ·ØÅŠ¶ĻĘ仹ŌŠŌĻą¶Ō“󊔣¬¢Ū“ķĪó£»·“Ó¦¢ņÖŠ£¬TiÓÉ£«4¼Ū½µµ½0¼Ū£¬ĆæÉś³É1 mol Ti(¼“48 g)×ŖŅĘ4 mol e££¬¹ŹĆæÉś³É19.2 g Ti(¼“0.4 mol)×ŖŅĘ1.6 mol e££¬½įŗĻ·“Ó¦¢ńĆæÉś³É0.4 mol TiCl4×ŖŅĘ1.6 mol e££¬·“Ó¦¢ń”¢¢ņÖŠ¹²×ŖŅĘ3.2 mol e££¬¢Ż“ķĪó”£
“š°ø””D



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
Ä³Ń§ÉśµÄŹµŃé±ØøęĖłĮŠ³öµÄĻĀĮŠŹż¾ŻÖŠŗĻĄķµÄŹĒ£Ø £©
A.ÓĆ10mLĮæĶ²ĮæČ”7.13mLĻ”ŃĪĖį
B.ÓĆĶŠÅĢĢģĘ½³ĘĮæ25.20g NaCl
C.ÓĆ¹ć·ŗpHŹŌÖ½²āµĆijČÜŅŗµÄpHĪŖ2.3
D.ÓĆ25mLµĪ¶Ø¹Ü×öÖŠŗĶµĪ¶ØŹ±£¬ÓĆČ„Ä³ÅØ¶ČµÄ¼īČÜŅŗ21.70mL
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÓĆŅ»¶ØĮæµÄSO2ŗĶO2ŌŚČŻ»ż¹Ģ¶ØµÄ2LĆܱÕČŻĘ÷ÄŚ·¢Éś·“Ó¦£ŗ2SO2+O2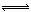 2SO3£¬Čē¹ū¦Ō(SO2)=0.05 mol/(L·min)£¬Ōņ2 minŗóSO3µÄĪļÖŹµÄĮæĪŖ
2SO3£¬Čē¹ū¦Ō(SO2)=0.05 mol/(L·min)£¬Ōņ2 minŗóSO3µÄĪļÖŹµÄĮæĪŖ
A£®0.1 mo1/L B£®0.2mol/L C£®0.1mol D£®0.2mol
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
Č”1mol¼×ĶéÓė4molĀČĘų·ÅČėŅ»ĆܱÕČŻĘ÷ÖŠ£¬ŌŚ¹āÕÕĢõ¼žĻĀ·¢Éś·“Ó¦£¬³ä·Ö·“Ó¦ŗó£¬ČŻĘ÷ÖŠø÷ĪļÖŹµÄĪļÖŹµÄĮæÖ®ŗĶŅ»¶ØĪŖ
A£®1mol B£®4mol C£®5mol D£®ĪŽ·ØČ·¶Ø
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠø÷×éĄė×ÓŅņ·¢ÉśŃõ»Æ»¹Ō·“Ó¦¶ų²»ÄÜ“óĮæ¹²“ęµÄŹĒ(””””)
A£®H£«”¢Fe2£«”¢Cr2O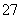 ”¢SO
ӢSO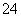
B£®Ca2£«”¢H£«”¢SO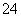 ”¢HCO
ӢHCO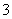
C£®Na£«”¢Ca2£«”¢Cl£”¢S2£
D£®Fe3£«”¢K£«”¢SCN£”¢Cl£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
Č”Ņ»¶ØĮæ µÄĖįŠŌKMnO4ČÜŅŗŅĄ“Ī½ųŠŠĻĀĮŠŹµŃ飬ӊ¹ŲĻÖĻó¼ĒĀ¼ČēĻĀ£ŗ
µÄĖįŠŌKMnO4ČÜŅŗŅĄ“Ī½ųŠŠĻĀĮŠŹµŃ飬ӊ¹ŲĻÖĻó¼ĒĀ¼ČēĻĀ£ŗ
¢ŁµĪ¼ÓŹŹĮæH2O2£¬×ĻŗģÉ«ĶĖČ„£¬²¢ÓŠĘųÅŻ²śÉś£»
¢ŚŌŁ¼ÓČėŹŹĮæµÄPbO2¹ĢĢ壬¹ĢĢåČܽā£¬ČÜŅŗÓÖ±äĪŖ×ĻŗģÉ«£»
¢Ū×īŗóĶØČė×ćĮæµÄSO2ĘųĢ唣
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)KMnO4”¢H2O2”¢PbO2Ńõ»ÆŠŌÓÉĒæµ½ČõµÄĖ³ŠņĪŖ____________________£»
(2)ŹµŃé¢ŪÖŠµÄĻÖĻóĪŖ_______________________________________________£»
(3)ŹµŃé¢Ł”¢¢ŚÖŠ·“Ó¦µÄĄė×Ó·½³ĢŹ½·Ö±šŹĒ________________________________
_____________ ___________________________________________________________ӣ
___________________________________________________________ӣ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
Ļņ200 mL 0.1 mol”¤L£1 FeCl2ČÜŅŗÖŠ¼ÓČėŹŹĮæNaOH£¬Ź¹Fe2£«Ē”ŗĆĶźČ«³Įµķ£¬Š”ŠÄ¼ÓČČ“Ė»ģŗĻĪļ£¬Ö±µ½Ė®·ÖÕōøÉ£¬Č»ŗó×ĘÉÕµ½ÖŹĮæ²»ŌŁ±ä»Æ£¬“ĖŹ±¹ĢĢåµÄÖŹĮæĪŖ(””””)”£
A£®1.6 g B£®2.34 g
C£®3.94 g D£®5.00 g
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠĶʶĻÕżČ·µÄŹĒ(””””)
A£®CO2”¢SO2”¢SO3”¢SiO2”¢NO2ŹĒĖįŠŌŃõ»ÆĪļ£¬ÄÜÓėNaOHČÜŅŗ·“Ó¦
B£®Na2O”¢Na2O2×é³ÉŌŖĖŲĻąĶ¬£¬ÓėCO2·“Ó¦²śĪļŅ²ĻąĶ¬
C£®CO”¢NO”¢NO2¶¼ŹĒ“óĘųĪŪČ¾ĘųĢ壬ŌŚæÕĘųÖŠ¶¼ÄÜĪČ¶Ø“ęŌŚ
D£®ŠĀÖĘĀČĖ®ĻŌĖįŠŌ£¬ĻņĘäÖŠµĪ¼ÓÉŁĮæ×ĻÉ«ŹÆČļŹŌŅŗ£¬³ä·ÖÕńµ“ŗóČÜŅŗĻȱäŗģŗóĶŹÉ«
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠ½āŹĶĪļÖŹÓĆĶ¾»ņĻÖĻóµÄ·“Ó¦·½³ĢŹ½²»×¼Č·µÄŹĒ
A£®ĮņĖįŠĶĖįÓźµÄŠĪ³É»įÉę¼°·“Ó¦£ŗ2H2SO3+O22H2SO4
B£®Čȵēæ¼īČÜŅŗæÉŅŌĒåĻ“ÓĶĪŪµÄŌŅņ£ŗ +2H2O
+2H2O H2CO3+2OH?
H2CO3+2OH?
C£®Ź¢·ÅNaOHČÜŅŗµÄŹŌ¼ĮĘæ²»ÄÜÓĆ²£Į§Čū£ŗSiO2+2OH?= +H2O
+H2O
D£®³É·ÖĪŖŃĪĖįµÄ½ą²ŽĮéÓė84Ļū¶¾Ņŗ»ģŗĻŹ¹ÓĆŅ×ÖŠ¶¾£ŗCl£+ ClO£+2H+= Cl2”ü+ H2O
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com