
某物质的实验式为PtCl4•2NH3,其水溶液不导电,加入AgNO3溶液反应也不产生沉淀,以强碱处理并没有NH3放出,则关于此化合物的说法中正确的是( )
|
| A. | 配合物中中心原子的电荷数和配位数均为6 |
|
| B. | 该配合物可能是平面正方形结构 |
|
| C. | Cl﹣ 和NH3分子均与Pt4+配位 |
|
| D. | 配合物中Cl﹣ 与Pt4+配位,而NH3分子不配位 |
考点:
配合物的成键情况.
专题:
化学键与晶体结构.
分析:
实验式为PtCl4•2NH3的物质,其水溶液不导电说明它不是离子化合物,在溶液中不能电离出阴、阳离子.加入AgNO3不产生沉淀,用强碱处理没有NH3放出,说明不存在游离的氯离子和氨分子,所以该物质的配位化学式为[PtCl4(NH3)2].
解答:
解:加入AgNO3不产生沉淀,用强碱处理没有NH3放出,说明不存在游离的氯离子和氨分子,所以该物质的配位化学式为[PtCl4(NH3)2],则
A.配合物中中心原子的电荷数电荷数为4,配位数为6,故A错误;
B.该配合物应是8面体结构,Pt与6个配体成键,故B错误;
C.由分析可知,Cl﹣和NH3分子均与Pt4+配位,形成的配合物为[PtCl4(NH3)2],故C正确;
D.用强碱处理没有NH3放出,说明NH3分子配位,故D错误.
故选C.
点评:
本题考查配合物知识,题目难度中等,解答本题的关键是能正确把握题给信息,注意配合物的形成特点.


 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案科目:高中化学 来源: 题型:
等体积的NaCl、MgCl2、AlCl3三种溶液分别与等体积等物质的量浓度的AgNO3溶液恰好完全反应,则NaCl、MgCl2、AlCl3三种溶液的物质的量浓度之比是()
A. 1:2:3 B. 3:2:1 C. 1:1:1 D. 6:3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
有关Na2CO3和NaHCO3的叙述中正确的是()
A. 相同质量的Na2CO3和NaHCO3与足量盐酸作用时,产生的气体质量相同
B. Na2CO3比NaHCO3热稳定性强
C. Na2CO3不能与澄清石灰水反应
D. Na2CO3和NaHCO3均可与NaOH溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
“类推”是一种常用的学习方法,但有时会产生错误的结论,下列类推结论中正确的是( )
|
| A. | ⅣA族元素氢化物沸点顺序是:GeH4>SiH4>CH4;则ⅤA族元素氢化物沸点顺序也是:AsH3>PH3>NH3 |
|
| B. | 第二周期元素氢化物的稳定性序是:HF>H2O>NH3;则第三周期元素氢化物的稳定性顺序也是:HCl>H2S>PH3 |
|
| C. | 晶体中有阴离子,必有阳离子;则晶体中有阳离子,必有阴离子 |
|
| D. | 干冰(CO2)是分子晶体,则SiO2也是分子晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关叙述正确的是( )
|
| A. | 已知NaH是离子化合物,则其电子式是 Na+[:H]﹣ |
|
| B. | 在PCl5分子中,磷原子满足最外层8电子结构 |
|
| C. | 在BCl3分子中,所有原子都满足最外层8电子结构 |
|
| D. | 石墨晶体是层状结构,在同一层上平均每个正六边形所含有的碳原子数为2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
I、卤素化学丰富多彩,能形成卤化物、卤素互化物、多卤化物等多种类型的化合物.
(1)①HClO4、②HIO4、③H5IO6 的酸性由强到弱的顺序为 (填序号).
(2)卤素互化物如BrI、ICl等与卤素单质结构相似、性质相近.Cl2、BrI、ICl沸点由高到低的顺序为 .
(3)气态氟化氢中存在二聚分子(HF)2,这是由于 .
(4)I3+(可看成II2+)属于多卤素阳离子,根据VSEPR模型推测I3+的空间构型为 .
(5)卤化物RbICl2加热时会分解为晶格能相对较大的卤化物A和卤素互化物或卤素单质,A的化学式为 .
II.氮可以形成多种离子,如N3﹣,NH2﹣,N3﹣,NH4+,N2H5+,N2H62+等,已知N2H5+与N2H62+是由中性分子结合质子形成的,类似于NH4+,因此有类似于 NH4+的性质.
(1)出N2H62+在足量碱性溶液中反应的离子方程式 .
(2)NH2﹣的电子式为 .
(3)写出两种由多个原子组成的含有与N3﹣电子数相同的物质的化学式 .
(4)等电子数的微粒往往具有相似的结构,试预测N3﹣的构型 .
(5)据报道,美国科学家1998年11月合成了一种名为“N5”的物质,由于其具有极强的爆炸性,又称为“盐粒炸弹”.迄今为止,人们对它的结构尚不清楚,只知道“N5”实际上是带正电荷的分子碎片,其结构是对称的,5个N排成V形.如果5个N结合后都达到8电子结构,且含有2个N≡N键.则“N5”分子碎片 所带电荷是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列萃取与分液相结合进行的操作(用苯从碘水中萃取碘单质,且已知苯的密度比水小)中错误的是()
A. 碘水和苯加入分液漏斗后,塞上上口部的塞子,用一手压住分液漏斗上口部,一手握住活塞部分,把分液漏斗倒转过来振荡,并不时地放气
B. 静置,待分液漏斗中液体分层后,先使分液漏斗内外空气相通(准备放出液体)
C. 打开分液漏斗的活塞,使全部下层液体沿承接液体的烧杯内壁慢慢流出,及时关闭活塞
D. 最后继续打开活塞,另用烧杯在分液漏斗的下口承接并保存上层液体
查看答案和解析>>
科目:高中化学 来源: 题型:
海洋植物如海带、海藻中含有丰富的碘元素,主要以碘化物形式存在.有一化学课外小组用海带为原料制取少量碘单质,他们将海带灼烧成灰,用水浸泡一段时间(以让碘化物充分溶解在水中),得到海带灰悬浊液,然后按以下实验流程提取单质碘:
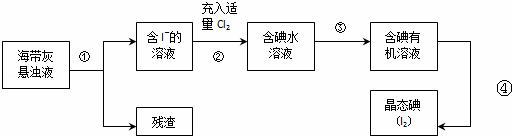
(1)步骤①需要用到的玻璃仪器(除烧杯外)还有
(2)指出提取碘的过程中有关的实验操作名称:③ .
查看答案和解析>>
科目:高中化学 来源: 题型:
完成并配平下列方程式(在横线上填写化学计量数,在方框内填写化学式):
Fe(OH)3+ +3KClO﹣ K2FeO4+ KCl+ H2O
(2)用一种试剂除去BaCl2溶液中含有的HCl,写出所用试剂及离子方程式.除杂试剂: .离子方程式
(3)鉴别饱和碳酸氢溶液和BaCl2溶液,可选用鉴别的试剂有(填编号) .
A.盐酸B.碳酸钠溶液C.澄清石灰水D.氨水
依次写出鉴别中有明显现象的反应的离子方程式 ;
少量澄清石灰水:
或过量澄清石灰水: .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com