
| A. | 某溶液中加入氯化钡溶液有白色沉淀生成,且沉淀不溶于稀盐酸,则原溶液一定含有SO42- | |
| B. | 某溶液中加入盐酸放出能使澄清的石灰水变浑浊的无色无味的气体,则原溶液一定含有CO32- | |
| C. | 检验某溶液中是否含有Fe3+时,可滴加硫氰化钾溶液,若溶液由无色变为血红色,则说明溶液中一定含有Fe3+ | |
| D. | 某溶液进行焰色反应,火焰颜色呈黄色,说明原溶液中一定不存在钾离子 |
分析 A.白色沉淀为AgCl或硫酸钡;
B.无色无味的气体为二氧化碳;
C.硫氰化钾与KSCN结合生成血红色的络离子;
D.火焰颜色呈黄色,一定含钠元素,观察K的焰色反应需要透过蓝色的钴玻璃.
解答 解:A.白色沉淀为AgCl或硫酸钡,且沉淀不溶于稀盐酸,则原溶液可能含有SO42-或银离子,但二者不能同时存在,故A错误;
B.无色无味的气体为二氧化碳,则原溶液可能含有CO32-或HCO3-,或二者都有,故B错误;
C.硫氰化钾与KSCN结合生成血红色的络离子,则溶液由无色变为血红色,则说明溶液中一定含有Fe3+,故C正确;
D.火焰颜色呈黄色,一定含钠元素,观察K的焰色反应需要透过蓝色的钴玻璃,则原溶液中一定含钠离子,不能确定是否含钾离子,故D错误;
故选C.
点评 本题考查常见离子的检验,为高频考点,把握离子检验的试剂、现象与结论为解答的关键,侧重分析与实验能力的考查,注意排除干扰离子,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 平衡后向容器中再充入与初始投料相同物质的量的CO2和H2,则CO的平衡浓度变为原来的2倍 | |
| B. | 恒温恒容下,增大压强,H2的浓度一定减小 | |
| C. | 升高温度,逆反应速率减小 | |
| D. | 该反应化学方程式为:CO2(g)+H2(g)?CO(g)+H2O(g)△H<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
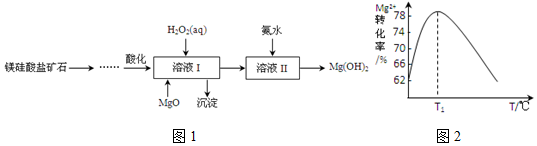
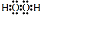 .溶液 I中加入H2O2溶液发生反应的离子方程式是2Fe2++H2O2+2H+=2Fe3++2H2O.
.溶液 I中加入H2O2溶液发生反应的离子方程式是2Fe2++H2O2+2H+=2Fe3++2H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用SO2漂白过的草帽日久会变色 | |
| B. | 用天燃气代替煤作燃料可减少大气污 | |
| C. | “84消毒液”杀死病菌是因为蛋白质变性 | |
| D. | 乙醇用作医用消毒剂时,无水乙醇消毒效果最好 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
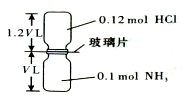 已知反应:HCl+NH3=NH4Cl(固体)如图所示,抽去装置中的玻璃片,使两种气体充分反应(整个过程中认为装置气密性良好),等温度恢复到原来温度.下列说法正确的是( )
已知反应:HCl+NH3=NH4Cl(固体)如图所示,抽去装置中的玻璃片,使两种气体充分反应(整个过程中认为装置气密性良好),等温度恢复到原来温度.下列说法正确的是( )| A. | 反应后瓶内压强是反应前的$\frac{1}{10}$ | |
| B. | 装置中氢元素的总质量为0.42 g | |
| C. | 生成物的分子数目为0.1 NA | |
| D. | 反应结束后,两个集气瓶很容易分开 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
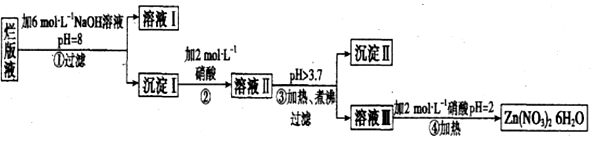
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 与等体积pH=11的NaOH溶液混合后所得溶液显酸性 | |
| B. | c(H+)=c(CH3COO-)+c(OH-) | |
| C. | 该溶液中由水电离出的c(H+)是1.0×10-11 mol/L | |
| D. | 加入少量CH3COONa固体后,c(CH3COO-)降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com