
 某学习小组依据氧化还原反应:2Ag++Cu═Cu2++2Ag设计成的原电池如图所示,则负极发生的电极反应为Cu-2e-═Cu2+;当反应进行到一段时间后取出电极材料,测得某一电极增重了5.4g,则该原电池反应共转移了的电子数目是0.05NA.
某学习小组依据氧化还原反应:2Ag++Cu═Cu2++2Ag设计成的原电池如图所示,则负极发生的电极反应为Cu-2e-═Cu2+;当反应进行到一段时间后取出电极材料,测得某一电极增重了5.4g,则该原电池反应共转移了的电子数目是0.05NA. 分析 根据总反应可知铜发生氧化反应,则铜失电子作原电池的负极;
Ag为原电池的正极,正极上发生还原反应,根据电极反应式计算转移电子的数目.
解答 解:在2Ag++Cu═Cu2++2Ag反应中,铜的化合价升高,发生氧化反应,则铜失电子作原电池的负极,电极反应为Cu-2e-═Cu2+;
原电池工作时,负极铜失去电子被氧化生成铜离子,铜的质量逐渐减少,溶液中的银离子在正极银得电子发生还原反应生成银,所以正极增重的质量就是析出银的质量,当银电极质量增加5.4g时,n(Ag)=$\frac{5.4g}{108g/mol}$=0.05mol,根据电极反应Ag++e-=Ag,可知原电池反应共转移电子的数目为0.05NA,
故答案为:Cu-2e-═Cu2+;0.05NA.
点评 本题考查了原电池设计,明确原电池原理是解本题关键,根据电池总反应式中得失电子的物质选取负极材料和电解质,知道原电池中正负极的判断方法,难度不大.


 全能练考卷系列答案
全能练考卷系列答案科目:高中化学 来源: 题型:解答题
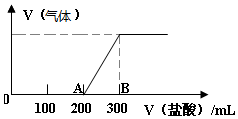 向100mL1.5mol/L的丙溶液中缓慢通入一定量的CO2,充分反应后,向所得溶液中逐滴缓慢滴加0.5mol/L的盐酸,所得气体的体积与所加盐酸的体积(不考虑气体溶解于水)关系如图所示.
向100mL1.5mol/L的丙溶液中缓慢通入一定量的CO2,充分反应后,向所得溶液中逐滴缓慢滴加0.5mol/L的盐酸,所得气体的体积与所加盐酸的体积(不考虑气体溶解于水)关系如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 13C与15N有相同的中子数 | B. | 13C与12C性质相同 | ||
| C. | 15N与14N互为同位素 | D. | 15N的核外电子数与中子数相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 22.4L氘(D2)气体,含有中子数为2NA | |
| B. | 1.6gNH2-离子所含电子数为NA | |
| C. | 4g氦气所含分子数为0.5NA | |
| D. | NA个SO3分子在标准状况下的体积为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A>B>C | B. | A>C>B | C. | C>B>A | D. | B>C>A |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
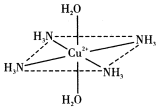 往硫酸铜水溶液中加入氨水,首先生成难溶物,继续加氨水,难溶物溶解,而且所得溶液的颜色比原来明显加深,得到了一种含2+的溶液,此离子的立体结构如图所示(4个NH3与Cu2+共面,跟H2O-Cu2+-H2O轴线垂直).请回答以下问题:
往硫酸铜水溶液中加入氨水,首先生成难溶物,继续加氨水,难溶物溶解,而且所得溶液的颜色比原来明显加深,得到了一种含2+的溶液,此离子的立体结构如图所示(4个NH3与Cu2+共面,跟H2O-Cu2+-H2O轴线垂直).请回答以下问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
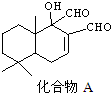 科学家研制出多种新型杀虫剂,以代替DDT.如图所示的化合物A就是其中的一种,下列关于化合物A的说法中正确的是( )
科学家研制出多种新型杀虫剂,以代替DDT.如图所示的化合物A就是其中的一种,下列关于化合物A的说法中正确的是( )| A. | 化合物A的分子式是C15H22O3 | |
| B. | 化合物A是芳香族化合物 | |
| C. | 化合物A可以发生卤代反应、酯化反应和银镜反应 | |
| D. | 1mol化合物A最多可与1molH2发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 选项 | 实验操作 | 实验目的或结论 |
| A | 向某盐溶液中加入AgNO3溶液,产生白色沉淀;加入浓NaOH溶液加热,生成使湿润红色石蕊试纸变蓝的气体 | 该盐一定是NH4Cl |
| B | 向浓硝酸中加入足量铜片充分反应,所得气体显红棕色 | 该气体是纯净的NO2 |
| C | 常温下,向浓度均为0.01mol/L的Na2CO3和Na2SO4的混合溶液中滴加1~2滴BaCl2溶液,滤出的沉淀不溶于盐酸 | 说明常温下Ksp(BaCO3)>Ksp(BaSO4) |
| D | 向Na2O2与水反应后所得溶液中加少量MnO2 | 检验Na2O2与水反应的中 间产物为H2O2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 将一定质量的镁和铝的混合物投入200mL稀硫酸中,固体全部溶解后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入的NaOH溶液体积的变化关系如图所示:
将一定质量的镁和铝的混合物投入200mL稀硫酸中,固体全部溶解后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入的NaOH溶液体积的变化关系如图所示:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com