
 如图是学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容,据此,完成下列问题:
如图是学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容,据此,完成下列问题: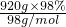 =9.2mol
=9.2mol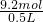 =18.4mol/L,
=18.4mol/L, 计算硫酸的物质的量;
计算硫酸的物质的量; 计算该硫酸试剂的物质的量浓度.
计算该硫酸试剂的物质的量浓度.

科目:高中化学 来源: 题型:解答题
 甲、乙、丙、丁是由短周期元素组成的物质,反应如下:甲+乙→丙+丁
甲、乙、丙、丁是由短周期元素组成的物质,反应如下:甲+乙→丙+丁 处.滴加浓氨水后试管内的现象:______反应化学方程式:______
处.滴加浓氨水后试管内的现象:______反应化学方程式:______查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
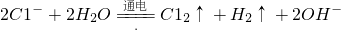
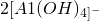
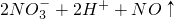
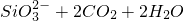 ═
═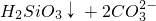
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
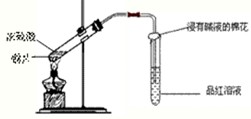 研究性学习小组为探究Cu与浓H2SO4反应及其产物SO2的性质,设计如下实验装置:
研究性学习小组为探究Cu与浓H2SO4反应及其产物SO2的性质,设计如下实验装置: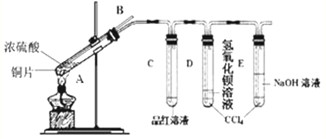
| 物质 | 溶解度(g/100水) | 物质 | 溶解度(g/100水) |
| Ca(OH)2 | 0.173 | Ba(OH)2 | 3.89 |
| CaCO3 | 0.0013 | BaSO3 | 0.016 |
| Ca(HCO3)2 | 16.60 |
| 实验方案 | 现象 |
| 1取少量溶液于试管中,加入氢氧化钠溶液 | |
| 2取少量溶液于试管中,加入稀盐酸,加热,用湿润的蓝色石蕊试纸检验生成的气体. |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com