
(7分)已知Ca(OH)2与Cl2反应的氧化产物与温度有关,在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应)。生成物中含有Cl 、ClO
、ClO 、
、 ;三种含氯元素的离子,其中C1O
;三种含氯元素的离子,其中C1O 、
、 两种离子的物质的量(n)与反应时间(t)的曲线如右图所示。
两种离子的物质的量(n)与反应时间(t)的曲线如右图所示。

(1)t1前,氧化产物是 (填化学式)。
(2)t2时,Ca(OH)2与Cl2发生反应的总的离子方程式为:
(3)该石灰乳中含有Ca(OH)2的物质的量是 mol
(4)NaClO2较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,其爆炸后的产物可能是 (填字母)。
A.NaCl、Cl2 B.NaCl、NaClO
C.NaClO3、NaClO4 D.NaCl、NaClO3
(5)配平下列离子方程式: Fe(OH)3+ ClO + OH
+ OH ————
————



(1)Ca(ClO)2 (1分)
(2) (2分)
(2分)
(3)5 (1分) (4)D (1分) (5)2, (5-n), 2n, (5-n) (n+3) (2分)
【解析】
试题分析:(1)Ca(ClO)2;t1时间,Cl2只有失去电子生成了ClO-
(2)  根据得失电子守恒进行配平,最后ClO-与ClO3-的比例符合2比1。生成物根据元素守恒判断,氯气的价态即能升高到+1价和+3价,还有降低到-1价,所以生成了Cl-。
根据得失电子守恒进行配平,最后ClO-与ClO3-的比例符合2比1。生成物根据元素守恒判断,氯气的价态即能升高到+1价和+3价,还有降低到-1价,所以生成了Cl-。
(3)根据方程式计算,有图像可知ClO-为2mol ,最后氯气过量,所以Ca(OH)2的物质的量是5mol。
(4)NaClO2中氯的价态是+3价,发生歧化反应,即升高价态生成 NaClO3又降低价态生成NaCl。
(5)根据得失电子守恒来配平,首先标出生成物 FeO4n-中Fe的价态为8-n,所以Fe变化的价态为8-n-3,即5-n。反应物中氯的价态为+1价,生成的氯为-1价,所以变化的价态为2,取最小公倍数2(5-n),所以反应物种氢氧化铁前面配2,氯气前面配(5-n),ClO-前面配(5-n)。最后根据O元素守恒,H元素守恒,OH 前面配2n,
前面配2n,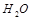 前面配n+3。
前面配n+3。
考点:氧化还原反应、离子反应方程式的书写。
点评:本题考查比较综合,难点在于离子反应方程式的书写,以及利用氧化还原反应中得失电子守恒的原理。


科目:高中化学 来源:2013届安徽省望江中学高三第一次月考化学试卷(带解析) 题型:填空题
(8分)已知Ca(OH)2与Cl2反应的氧化产物与温度有关,在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应)。生成物中含有Cl—、ClO—、ClO3—三种含氯元素的离子,其中ClO—、ClO3—两种离子的物质的量(n)与反应时间(t)的曲线如图所示。
(1)t1前,氧化产物是________(填化学式)。
(2)t2时,Ca(OH)2与Cl2发生反应的总的离子方程式为: 。
(3)该石灰乳中含有Ca(OH)2的物质的量是 mol。
(4)NaClO2较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,其爆炸后的产物可能是 。
| A.NaCl、Cl2 | B.NaCl、NaClO | C.NaClO3、NaClO4 | D.NaCl、NaClO3 |
查看答案和解析>>
科目:高中化学 来源:2013届江西省江西师大附中、临川一中高三12月联考化学试卷(带解析) 题型:填空题
(7分)已知Ca(OH)2与Cl2反应的氧化产物与温度有关,在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应)。生成物中含有Cl 、ClO
、ClO 、
、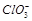 ;三种含氯元素的离子,其中C1O
;三种含氯元素的离子,其中C1O 、
、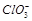 两种离子的物质的量(n)与反应时间(t)的曲线如右图所示。
两种离子的物质的量(n)与反应时间(t)的曲线如右图所示。
(1)t1前,氧化产物是 (填化学式)。
(2)t2时,Ca(OH)2与Cl2发生反应的总的离子方程式为:
(3)该石灰乳中含有Ca(OH)2的物质的量是 mol
(4)NaClO2较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,其爆炸后的产物可能是 (填字母)。
| A.NaCl、Cl2 | B.NaCl、NaClO |
| C.NaClO3、NaClO4 | D.NaCl、NaClO3 |
 + OH
+ OH ————
———— 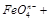
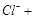
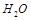
查看答案和解析>>
科目:高中化学 来源:2013-2014学年四川省高三“联测促改”活动理综化学试卷(解析版) 题型:实验题
某研究性学习小组对还原铁粉与水蒸气的反应产物进行科学探究。已知Ca(OH)2的分解温度为580℃,铁粉与水蒸气反应的温度为900℃:根据下图所示实验装置,进行了还原铁粉与水蒸气的反应实验,实验中观察到肥皂液中产生了大量的气泡。

(1)实验中Ca(OH)2的作用是 。实验中产生的气体产物是 。
(2)为进一步探究还原铁粉与水蒸气反应固体产物的成分,研究性学习小组将反应后的固体经处理后得到黑色氧化物固体,针对黑色氧化物固体,该小组提出如下的假设并进行了相关的实验:
假设一:固体为FeO
假设二:固体为Fe3O4
假设三:
①限选用下列试剂:盐酸、KSCN溶液、K3Fe(CN)6 溶液、氯水,证明假设一不成立
|
操作 |
现象 |
结论 |
|
|
|
假设一不成立 |
②为了进一步确定产物的成分,用黑色固体进行了下列实验:

加入足量氯水所发生反应的离子方程式是 ;检验红褐色固体是否洗涤干净的操作是 ;灼烧时盛放固体的仪器是 ;若假设二成立,黑色固体最终全部转化成的红棕色粉末的质量是 g
查看答案和解析>>
科目:高中化学 来源:2012-2013学年安徽省高三第一次月考化学试卷(解析版) 题型:填空题
(8分)已知Ca(OH)2与Cl2反应的氧化产物与温度有关,在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应)。生成物中含有Cl—、ClO—、ClO3—三种含氯元素的离子,其中ClO—、ClO3—两种离子的物质的量(n)与反应时间(t)的曲线如图所示。

(1)t1前,氧化产物是________(填化学式)。
(2)t2时,Ca(OH)2与Cl2发生反应的总的离子方程式为: 。
(3)该石灰乳中含有Ca(OH)2的物质的量是 mol。
(4)NaClO2较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,其爆炸后的产物可能是 。
A.NaCl、Cl2 B. NaCl、NaClO C.NaClO3、NaClO4 D. NaCl、NaClO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com