
将等物质的量的镁和铝混合,取等质量该混合物四份,分别加到足量的下列溶液中,充分反应后,放出氢气最多的是( )
A.3 mol·L-1 HCl B.4 mol·L-1 HNO3
C.8 mol·L-1 NaOH D.18 mol·L-1 H2SO4
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源:2015-2016学年四川省成都市高一下4月月考化学试卷(解析版) 题型:选择题
 O2气体,不久前在我国兰州近代物理研究所制备成功,1mol 这种
O2气体,不久前在我国兰州近代物理研究所制备成功,1mol 这种 O2气体所含有的中子的物质的量为( )
O2气体所含有的中子的物质的量为( )
A. 36 mol B. 20 mol C. 16 mol D. 20 NA
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西大学附中高二下3月月考化学试卷(解析版) 题型:选择题
已知1~18号元素的离子aW3+、bX+、cY2﹣、dZ﹣都具有相同的电子层结构,下列关系正确的是( )
A. 质子数c>d,离子的还原性Y2﹣>Z﹣
B. 氢化物的稳定性H2Y>HZ
C. 原子半径X<W,第一电离能X<W
D. 电负性Z>Y>W>X
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西重点中学协作体高二下学期期末化学试卷(解析版) 题型:填空题
锶(Sr)为第五周期ⅡA族元素,其化合物六水氯化锶(SrCl2·6H2O)是实验室重要的分析试剂,工业上常以天青石(主要成分为SrSO4)为原料制备,生产流程如下:
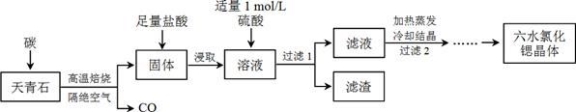
已知:① 经盐酸浸取后,溶液中除含有Sr2+和Cl-外,还含有少量Ba2+杂质;
② SrSO4、BaSO4的溶度积常数分别为3.3×10-7、1.1×10-10;
③ 六水氯化锶晶体61℃时开始失去结晶水,100℃时失去全部结晶水。
(1)天青石焙烧前先研磨粉碎,其目的是_________________________________________。
(2)天青石和碳隔绝空气高温焙烧时 SrSO4中只有S被还原,且1 mol SrSO4反应电子转移8 mol,该反应的化学方程式_____________________________________________。
(3)“滤渣”是 。(写化学式)
(4)为了得到较纯的六水氯化锶晶体,“过滤2”后需经过“洗涤,干燥”的操作:
① 洗涤氯化锶晶体最好选用饱和氯化锶溶液,其原因是 。
② 工业上用热风吹干六水氯化锶,选择的适宜温度范围是 (填字母)。
A.50~60℃ | B.70~80℃ | C.80~100℃ | D.100℃以上 |
(5)产品纯度检测:称取1.000 g产品溶解于适量水中,向其中加入含AgNO3 1.100×10-2mol的AgNO3溶液(此时溶液中除Cl―外,不含其它与Ag+反应的离子),待Cl―完全沉淀后,用含Fe3+的溶液作指示剂,用0.2000 mol/L的NH4SCN标准溶液滴定剩余的AgNO3,使剩余的Ag+ 以AgSCN白色沉淀的形式析出,滴定达到终点的现象是________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西重点中学协作体高二下学期期末化学试卷(解析版) 题型:选择题
可用于鉴别以下三种化合物的试剂组合是( )
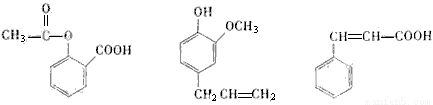
乙酰水杨酸 丁香酚 肉桂酸
①银氨溶液 ②溴的四氯化碳溶液 ③氯化铁溶液 ④碳酸钠溶液
A.②与③ B.③与④ C.①与④ D.②与④
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西重点中学协作体高二下学期期末化学试卷(解析版) 题型:选择题
某溶液既能溶解Al(OH)3,又能溶解Al,但不能溶解Fe,在该溶液中可以大量共存的离子组是( )
A.K+、Na+、HCO3-、NO3-
B.Na+、SO42-、Cl-、S2-
C.NH4+、Mg2+、SO42-、NO3-
D.H+、K+、Cl-、Na+
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省资阳市高二下学期期末化学试卷(解析版) 题型:填空题
某研究性学习小组将甲、乙、丙装置连接如图,除G、H外所有电极均为惰性电极。电解一段时间后,D电极质量增加。试回答下列问题:
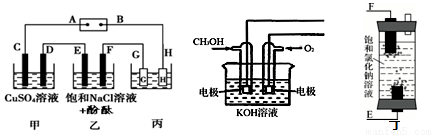
(1)电源A极是____极(填“正”或“负”);乙装置F电极附近的现象是____。
(2)欲用丙装置给铜镀银。G应该是____(填“Ag”或“Cu”)。
(3)如用甲醇燃料电池(如图)充当电源,写出负极的电极反应方程式:____;若用丁装置(如图)代替乙装置,写出丁装置中反应的总化学方程式是____。
查看答案和解析>>
科目:高中化学 来源:2016年全国普通高等学校招生统一考试化学(北京卷精编版) 题型:简答题
用零价铁(Fe)去除水体中的硝酸盐(NO3-)已成为环境修复研究的热点之一。
(1)Fe还原水体中NO3-的反应原理如图所示。
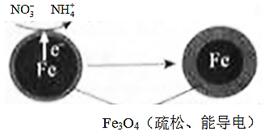
①作负极的物质是________。
②正极的电极反应式是_________。
(2)将足量铁粉投入水体中,经24小时测定NO3—的去除率和pH,结果如下:
初始pH | pH=2.5 | pH=4.5 |
NO3—的去除率 | 接近100% | <50% |
24小时pH | 接近中性 | 接近中性 |
铁的最终物质形态 |
|
|
pH=4.5时,NO3—的去除率低。其原因是________。
(3)实验发现:在初始pH=4.5的水体中投入足量铁粉的同时,补充一定量的Fe2+可以明显提高NO3—的去除率。对Fe2+的作用提出两种假设:
Ⅰ. Fe2+直接还原NO3—;
Ⅱ. Fe2+破坏FeO(OH)氧化层。
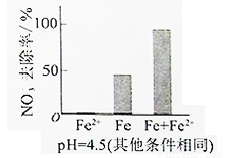
①做对比实验,结果如图所示,可得到的结论是_______。
②同位素示踪法证实Fe2+能与FeO(OH)反应生成Fe3O4。结合该反应的离子方程式,解释加入Fe2+提高NO3—去除率的原因:______。
(4)其他条件与(2)相同,经1小时测定NO3—的去除率和pH,结果如下:
初始pH | pH=2.5 | pH=4.5 |
NO3—的去除率 | 约10% | 约3% |
1小时pH | 接近中性 | 接近中性 |
与(2)中数据对比,解释(2)中初始pH不同时,NO3—去除率和铁的最终物质形态不同的原因:__________。
查看答案和解析>>
科目:高中化学 来源:2016年全国普通高等学校招生统一考试化学(新课标1卷精编版) 题型:选择题
短周期元素W、X、Y、Z的原子序数依次增加。m、p、r是由这些元素组成的二元化合物,n是元素Z的单质,通常为黄绿色气体,q的水溶液具有漂白性,0.01 mol·L–1r溶液的pH为2,s通常是难溶于水的混合物。上述物质的转化关系如图所示。下列说法正确的是( )
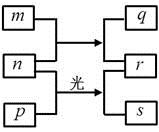
A. 原子半径的大小W<X<Y
B. 元素的非金属性Z>X>Y
C. Y的氢化物常温常压下为液态
D. X的最高价氧化物的水化物为强酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com