
【题目】下列各组物质能用分液漏斗分离的是( )
A.植物油和水的混合物
B.含泥沙的食盐水
C.乙醇的水溶液
D.硫酸钡和氯化银的固体混合物
科目:高中化学 来源: 题型:
【题目】(1)某学生用0.1500 mol/L NaOH溶液测定某未知浓度的盐酸溶液,其操作可分解为如下几步:
A.用蒸馏水洗净滴定管
B.用待测定的溶液润洗酸式滴定管
C.用酸式滴定管取稀盐酸25.00 mL,注入锥形瓶中,加入酚酞
D.另取锥形瓶,再重复操作2~3次
E.检查滴定管是否漏水
F.取下碱式滴定管用标准NaOH溶液润洗后,将标准液注入碱式滴定管“0”刻度以上2~3 cm处,再把碱式滴定管固定好,调节液面至“0”刻度或“0”刻度以下
G.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度
完成以下填空:
(1)滴定时正确操作的顺序是(用序号字母填写):____→ → F → → → → D。
(2)操作F中应该选择图中滴定管_____(填标号)。
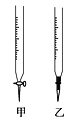
(3)滴定时边滴边摇动锥形瓶,眼睛应注意观察_____。
(4)滴定结果如表所示:
滴定次数 | 待测液体积/mL | 标准溶液的体积/mL | |
滴定前刻度 | 滴定后刻度 | ||
1 | 25.00 | 1.02 | 21.03 |
2 | 25.00 | 0.60 | 20.60 |
3 | 25.00 | 0.20 | 20.19 |
计算该盐酸的物质的量浓度为_____(精确至0.0001)。
(5)下列操作会导致测定结果偏高的是_____。
A.碱式滴定管在装液前未用标准NaOH溶液润洗
B.滴定过程中,锥形瓶摇荡得太剧烈,锥形瓶内有液滴溅出
C.碱式滴定管尖嘴部分在滴定前没有气泡,滴定终点时发现气泡
D.达到滴定终点时,仰视读数
(6)氧化还原滴定实验与酸碱中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。测血钙的含量时,进行如下实验:
①可将2mL血液用蒸馏水稀释后,向其中加入足量草酸铵(NH4)2C2O4晶体,反应生成 CaC2O4沉淀,将沉淀用稀硫酸处理得H2C2O4溶液。
②将①得到的H2C2O4溶液,再用酸性KMnO4溶液滴定,氧化产物为CO2,还原产物为Mn2+。
③终点时用去20mL l.0×l0﹣4 mol/L的KMnO4溶液。
Ⅰ、写出用KMn04滴定H2C2O4的离子方程式_____________________。
Ⅱ、判断滴定终点的方法是________________________。
Ⅲ、计算:血液中含钙离子的浓度为_____mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在反应3BrF3+5H2O===HBrO3+Br2+9HF+O2↑中,若有5 mol H2O作为还原剂时,被还原的BrF3的物质的量为( )
A. 3 mol B. 2 mol C. ![]() mol D.
mol D. ![]() mol
mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W、R为原子序数依次增大的短周期元素。化合物甲由X、Z、W三种元素组成,常温下0.1mol·L-1甲溶液的pH=13。工业上常通过电解饱和WR溶液制得甲。Y的单质与由Y、Z组成的化合物之间的转化关系如图所示。下列叙述正确的是( )
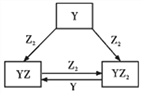
A. 简单离子的半径:W>Z>R B. 化合物W2Z2中既含离子键又含极性键
C. 化合物YZ2溶于足量甲溶液中,存在的微粒有6种 D. 图中转化过程发生的反应均为化合反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据权威刊物报道,1996年科学家在宇宙中发现H3分子。甲、乙、丙、丁四位学生对此报道的认识正确的是
A.甲认为上述发现绝对不可能,因为H3分子违背了共价键理论
B.乙认为宇宙中还可能存在另一种氢单质,因为氢元素有三种同位素必然有三种同素异形体
C.丙认为H3分子实质上是H2分子与H+以特殊共价键结合的产物,应写成H
D.丁认为如果上述的发现存在,则证明传统的价键理论有一定的局限性有待继续发展
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氰气的分子式为(CN)2,结构式为N![]() C-C
C-C![]() N,性质与卤素相似,下列叙述正确的是
N,性质与卤素相似,下列叙述正确的是
A. 分子中四原子共直线,是非极性分子 B. N![]() C 键的键长大于C
C 键的键长大于C![]() C键的键长
C键的键长
C. 分子中含有2个σ键和4个π键 D. 氰气不和氢氧化钠溶液发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室里需要纯净的氯化钠晶体,但现在只有混有硫酸钠、碳酸氢铵的氯化钠。某学生设计了如下方案:
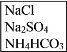
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
请回答下列问题:
(1)操作①加热的目的是________________,
(2)操作②除用BaCl2溶液外,还可用____________替代。
(3)操作②,判断SO42-已除尽的方法是________________________。
(4)操作③的目的是____________,不先过滤后再加Na2CO3溶液的理由是____________。
(5)操作④的名称是______________,应在________(填仪器名称)中进行。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨氯地平可用于治疗高血压和心绞痛。其中间体F的合成路线流程图如下:
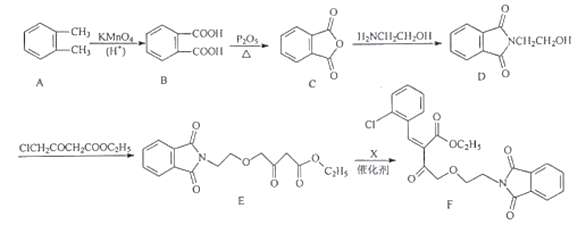
(1)F中的含氧官能团名称为酰胺键、________和________等。
(2)D![]() E的反应类型为___________
E的反应类型为___________
(3)X的分子式为C7H5Ocl,写出X的结构简式:___________
(4)写出同时满足下列条件的E的一种同分异构体的结构简式:___________
①含两个苯环的α-氨基酸②能与FeCl3溶液发生显色反应③分子中只有5种不同化学环境的氢
(5)已知:CH3CH2CN![]() CH3CH2COOH。请写出以CH3CH2OH、NCCH2CN、
CH3CH2COOH。请写出以CH3CH2OH、NCCH2CN、![]() 为原料制备
为原料制备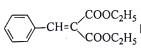 的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。____________
的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。____________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com