
| A、2 I-+Cl2→I2+2Cl- |
| B、2Fe2++2I-+2Cl2→2Fe3++I2+4Cl- |
| C、2Fe2++4I-+3Cl2→2Fe3++2I2+6Cl- |
| D、2Fe2++6I-+4Cl2→2Fe3++3I2+8Cl- |


科目:高中化学 来源: 题型:
| A、在蔗糖中加入浓H2SO4后出现发黑现象,说明浓硫酸具有吸水性 |
| B、浓硝酸保存在棕色的细口瓶中,并置于低温阴暗处 |
| C、金属钠着火燃烧时,可用泡沫灭火器灭火 |
| D、正常雨水pH等于7,酸雨的pH小于7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | 结构或性质信息 |
| T | 基态原子的L层上s电子数等于p电子数 |
| X | 基态原子的最外层未成对电子数在该元素所在周期中最多 |
| Y | 基态原子的第一电离能在该元素所在周期中最小 |
| Z | 单质常温、常压下是气体.基态原子的M层上有1个未成对的p电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
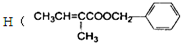 是一种的香精素,有关合成路线如下:
是一种的香精素,有关合成路线如下: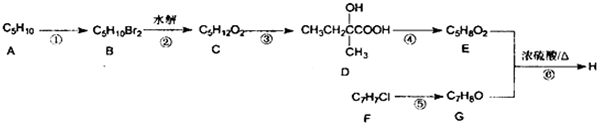
查看答案和解析>>
科目:高中化学 来源: 题型:
| 滴定序号 | 待测溶液体积(单位:mL) | 所消耗盐酸体积(单位:mL) | ||
| 滴定前读数 | 滴定后读数 | 消耗盐酸体积 | ||
| 1 | 20.00 | 0.50 | 20.60 | V(平)= |
| 2 | 20.00 | 6.00 | 26.00 | |
| 3 | 20.00 | 4.50 | 24.50 | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com