
【题目】①Cu丝 ②Cl2 ③Al2(SO4)3溶液 ④蔗糖 ⑤浓硝酸⑥Ca(OH)2⑦NH4Cl⑧CO2 ⑨氨水
请用以上相应的数字编号和化学用语回答问题:
(1)属于电解质的是__________;属于非电解质的是__________.
(2)实验室制取氨气的化学反应方程式_______________________.
(3)工业制漂白粉的化学反应方程式__________________________.
(4)实验室制Al(OH)3的离子方程式______________________________________________________
(5)①和⑤的化学方程式并用双线桥标出电子转移__________.
【答案】⑥⑦ ④⑧ 2NH4Cl + Ca(OH)2 ![]() CaCl2 + 2NH3↑+ 2H2O 2Cl2 + 2Ca(OH)2 = CaCl2 + Ca(ClO)2 + 2H2O Al3+ + 3NH3·H2O = Al(OH)3↓ + 3NH4+
CaCl2 + 2NH3↑+ 2H2O 2Cl2 + 2Ca(OH)2 = CaCl2 + Ca(ClO)2 + 2H2O Al3+ + 3NH3·H2O = Al(OH)3↓ + 3NH4+ 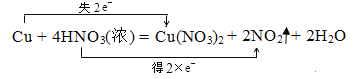
【解析】
(1)根据电解质与非电解质的定义判断。电解质:在水溶液中或熔融状态下能够导电的化合物;非电解质:在熔融状态和水溶液中都不能导电的化合物;单质和混合物既不是单质,也不是非电解质。
(2)实验室用固体氢氧化钙与氯化铵制备氨气;
(3)工业上用氯气与石灰乳(溶质为氢氧化钙)制备漂白粉;
(4)实验室利用硫酸铝与氨水制备Al(OH)3沉淀;
(5)①和⑤反应会生成硝酸铜、二氧化氮与水,根据氧化还原反应的规律,按“标价态”——“连双线”——“注得失”的顺序标出电子得失情况。
①Cu丝为单质,既不是电解质,也不是非电解质;
②Cl2为单质,既不是电解质,也不是非电解质;
③Al2(SO4)3溶液为混合物,既不是电解质,也不是非电解质;
④蔗糖为有机物,在水溶液和熔融状态下不导电,故蔗糖为非电解质;
⑤浓硝酸为浓度较高的硝酸的水溶液,是混合物,故浓硝酸既不是电解质,也不是非电解质;
⑥Ca(OH)2是化合物,溶于水或熔融状态下均会电离出自由移动的离子,则Ca(OH)2是电解质;
⑦NH4Cl在水溶液中能电离出自由移动的铵根离子和氯离子,则NH4Cl是电解质;
⑧CO2为化合物,溶于水后形成碳酸,但自身不能电离出自由移动的离子,故CO2为非电解质;
⑨氨水为一水合氨的水溶液,为混合物,故氨水既不是电解质,也不是非电解质;
故属于电解质的为:⑥⑦;非电解质的为:④⑧,
答案为:⑥⑦;④⑧;
(2)实验室制取氨气的化学反应方程式:2NH4Cl + Ca(OH)2 ![]() CaCl2 + 2NH3↑+ 2H2O,
CaCl2 + 2NH3↑+ 2H2O,
故答案为:2NH4Cl + Ca(OH)2![]() CaCl2 + 2NH3↑+ 2H2O;
CaCl2 + 2NH3↑+ 2H2O;
(3)工业上用氯气与氢氧化钙反应制取漂白粉,其化学方程式为:2Cl2 + 2Ca(OH)2 = CaCl2 + Ca(ClO)2 + 2H2O,
故答案为:2Cl2 + 2Ca(OH)2 = CaCl2 + Ca(ClO)2 + 2H2O;
(4)实验室利用硫酸铝与氨水反应制取Al(OH)3,其离子方程式为:Al3+ + 3NH3·H2O = Al(OH)3↓ + 3NH4+,
故答案为:Al3+ + 3NH3·H2O = Al(OH)3↓ + 3NH4+;
(5)铜与浓硝酸反应生成硝酸铜、二氧化氮和水,用双线桥法表示电子转移数目如下:
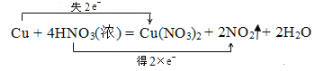 ,
,
故答案为: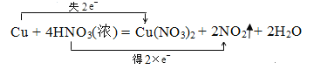 。
。


 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 节日里燃放的五彩缤纷的烟花是某些金属元素化学性质的展现
B. 将等物质的量的氧化钠和过氧化钠分别投入到足量且等质量的水中,得到溶质质量分数分别是 a%和 b%的两种溶液,则a 和 b 的关系是 a=b
C. 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热,熔化后的液态铝滴落下来, 说明金属铝的熔点较低
D. 用如图装置进行实验,将装置①中的 AlCl3 溶液滴入装置②浓氢氧化钠溶液,溶液中可观察到有大量白色沉淀产生

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取一定量的Na2CO3和NaHCO3固体混合物加热至无气体放出为止,称得加热后剩余固体质量比原来减少了6.2 g,现再取同样质量的原固体混合物与过量的盐酸反应,生成15.68 L CO2(标准状况)。请计算:
(1)加热后剩余固体物质的成分是什么_________?
(2)混合物中Na2CO3和NaHCO3的物质的量分别是多少______________?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定质量Fe2O3和Al2O3的混合固体溶解在200mL 0.1mol·L-1的过量H2SO4溶液中,然后向其中加入NaOH溶液使Fe3+、Al3+刚好完全沉淀,用去NaOH溶液100 mL,则NaOH溶液的浓度为
A. 0.4 mol·L-1 B. 0.2 mol·L-1
C. 0.1 mol·L-1 D. 0.8 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH2OH(羟胺)是一种无色针状结晶,羟胺及其盐类常用作有机合成的还原剂。回答下列问题:
(1) NH2OH的电子式为________________。
(2)拉西法制备羟胺的总反应为2NO2-+4SO2+6H2O+6NH3=4SO42-+6NH4++2NH2OH。该反应中NH3__________(填“作氧化剂”“作还原剂”或“既不作氧化剂又不作还原剂”)。
(3)室温时,NH2OH会发生分解反应,分解产生的无色气体遇浓盐酸产生白烟,与空气接触变为红棕色;且其分解产物会使无水CuSO4变蓝色,则NH2OH分解反应的化学方程式为______________________。
(4)催化还原NO是制备盐酸羟胺的一种方法,其反应原理如下:2NO+3H2+2HCl![]() 2NH2OH·HCl,某校合作学习小组的同学设计了如图所示装置制备盐酸羟胺:
2NH2OH·HCl,某校合作学习小组的同学设计了如图所示装置制备盐酸羟胺:

①该实验适宜的加热方式为______________。
②装置中导管X的作用是_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低.某同学取一定量的铝铁合金与100mL很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入4 mol/L的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示.试回答下列问题:
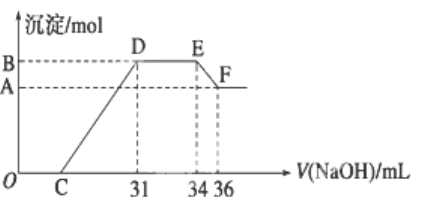
(1)结合OH-的能力最弱的是________(填离子符号)
(2)B与A的差值为________mol.
(3)原混合物中铝粉与铁粉的物质的量之比为______.
(4)B点对应的沉淀量为________mol,C点对应的溶液体积为________mL.
(5)硝酸溶液的物质的量浓度为_________mol·L-1
(6)写出铝与该浓度硝酸反应的离子方程式_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在元素周期表前四周期中原子序数依次增大的六种元素A、B、C、D、E、F中,A与其余五种元素既不同周期也不同主族,B的一种核素在考古时常用来鉴定一些文物的年代,C的氧化物是导致酸雨的主要物质之一,D原子核外电子有8种不同的运动状态,E的基态原子在前四周期元素的基态原子中单电子数最多,F元素的基态原子最外能层只有一个电子,其它能层均已充满电子.
(1)写出基态E原子的价电子排布式 .
(2)B、C、D三元素第一电离能由小到大的顺序为(用元素符号表 示) ;A与C形成CA3型分子,分子中C原子的杂化类型为 ,分子的立体结构为 ;C的单质与 BD化合物是等电子体,据等电子体的原理,写出BD化合物的电子式 ; A2D由液态形成晶体时密度 (填增大,不变或减小),分析主要原因(用文字叙述)
(3)已知D、F能形成一种化合物,其晶胞的结构如图所示,则该化合物的化学式为(用元素符号表示) ;若相邻D原子和F原子间的距离为a cm,阿伏伽德罗常数为NA,则该晶体的密度为 g/cm3(用含a、NA的符号表示).

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质均为a g,将它们在氧气中完全氧化的产物全部通入到足量的过氧化钠固体中,过氧化钠固体增重为a g,符合条件的物质种类有( )
①CO ②H2 ③CH4 ④HCHO ⑤CH3COOH ⑥HCOOH
A. 4 种 B. 5 种 C. 6种 D. 2种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室通常采用以下装置来制备纯净干燥的氯气,回答下列问题:
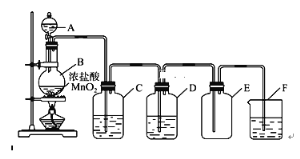
(1)写出实验室制备氯气的化学反应方程式:____________________________________。
(2)在反应中MnO2发生______(填“氧化”或“还原”,下同)反应,Cl2是______产物。
(3)装置C中所装试剂为________,其作用为_______________________________。
(4)检验氯气是否收集满的方法为:_________________________________________。
(5)F中反应的离子反应方程式为_________________________________________。
(6)工业上常用氯气与石灰水反应制备漂白粉,而久置漂白粉容易失效,请写出漂白粉失效的原理____________________________,_______________________________(用化学方程式表示)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com