
分析 ①目前计入空气污染指数的项目暂定为:二氧化硫、氮氧化物和总悬浮颗粒物等,以此来解答;
②煤中含有硫,燃烧时能生成二氧化硫,二氧化硫能和氧化钙反应;
③甲醛是来自人造地板、家具以及装修粘合剂,长期接触低剂量的该物质,免疫功能异常;天然大理石含有放射性元素氡;
④混凝剂、活性炭能够起到吸附沉淀作用;ClO2具有强的氧化性能够杀菌消毒.
解答 解:①目前计入空气污染指数的项目暂定为:二氧化硫、氮氧化物和总悬浮颗粒物等;
故答案为:氮的氧化物;
②煤燃烧过程中能生成二氧化硫,二氧化硫有毒,能污染环境,生石灰能够和生成的二氧化硫反应,从而防止二氧化硫污染空气;
故答案为:CaCO3或CaO;
③甲醛是来自人造地板、家具以及装修粘合剂,长期接触低剂量的该物质,免疫功能异常;天然大理石含有放射性元素氡;
故答案为:甲醛;氡;
④自来水生产过程中通常要经过加入混凝剂、活性炭和ClO2等物质的处理,每种物质主要作用分别是除去固体杂质和悬浮物、吸附某些溶解的杂质并除去水中异味、杀菌消毒;
故答案为:杀菌消毒.
点评 本题考查了生活中的化学知识,设计环境污染与治理、室内环境污染源、自来水的净化,侧重考查学生对基础知识掌握的熟练程度,题目难度不大,注意对相关知识的积累.


 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案科目:高中化学 来源: 题型:选择题
| A. | 3.4g H2O2中含有的共用电子对数为0.1NA | |
| B. | 25℃,pH=13的NaOH溶液中,含有OH-的数目为0.1NA | |
| C. | 标准状况下,2.24L氯气溶于水发生反应,转移的电子数目为0.1 NA | |
| D. | 标况下,11.2 L由CH4和C2H4组成的混合气体中含有氢原子的数目为2 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
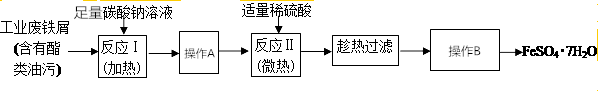
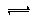 HCO3-+OH-,溶液呈碱性,酯在碱性条件下完全水解(结合离子方程式解释),反应Ⅰ需要加热,其原因是升高温度,促进水解,溶液碱性增强,使反应充分进行.
HCO3-+OH-,溶液呈碱性,酯在碱性条件下完全水解(结合离子方程式解释),反应Ⅰ需要加热,其原因是升高温度,促进水解,溶液碱性增强,使反应充分进行.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化铝溶液与过量的氨水反应:Al3++3OH-═Al(OH)3↓ | |
| B. | 钠和硫酸铜溶液的反应:2Na+Cu2+═2Na++Cu | |
| C. | 铜与浓硝酸反应:Cu+NO3-+4H+═Cu2++NO2↑+2H2O | |
| D. | 氯气与水反应:Cl2+H2O?H++Cl-+HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
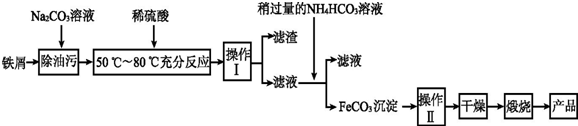
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学反应速率是衡量化学反应进行快慢程度的物理量 | |
| B. | 化学反应速率通常用单位时间内生成或消耗某物质的质量的多少来表示 | |
| C. | 在同一个反应中,用各物质表示的反应速率之比等于其化学方程式中的化学计量数之比 | |
| D. | 化学反应速率的常用单位有mol•L-1•s-1和mol/(L•min) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com