
| A. | 10 min内,Y的平均反应速率为0.03 mol•L-1•s-1 | |
| B. | 10 min内,X和Y反应放出的热量为a kJ | |
| C. | 10 min内,消耗0.2 mol X,生成0.4 mol Z | |
| D. | 10 min内,前5minX的平均反应速率与后5minX的平均反应速率相同 |
分析 将1mol X和3mol Y通入2L的恒容密闭容器中,反应10min,测得Y的物质的量为2.4mol,则
X(g)+3Y(g)?2Z(g)
开始 1 3 0
转化 0.2 0.6 0.4
平衡 0.8 2.4 0.4
结合v=$\frac{△c}{△t}$、物质的量与热量成正比计算.
解答 解:将1mol X和3mol Y通入2L的恒容密闭容器中,反应10min,测得Y的物质的量为2.4mol,则
X(g)+3Y(g)?2Z(g)
开始 1 3 0
转化 0.2 0.6 0.4
平衡 0.8 2.4 0.4
A.10 min内,Y的平均反应速率为$\frac{\frac{0.6mol}{2L}}{600s}$=0.0005mol•L-1•s-1,故A错误;
B.1molX完全反应放出热量为akJ,则10 min内,X和Y反应放出的热量为0.2a kJ,故B错误;
C.X、Z的物质的量比为1:2,则10 min内,消耗0.2 mol X,生成0.4 mol Z,故C正确;
D.浓度越大,反应速率越快,则前5minX的平均反应速率大于后5minX的平均反应速率,故D错误;
故选C.
点评 本题考查化学平衡的计算,为高频考点,把握化学平衡三段法、速率及热量的计算为解答的关键,侧重分析与计算能力的考查,注意选项D为解答的难点,题目难度不大.


科目:高中化学 来源: 题型:选择题
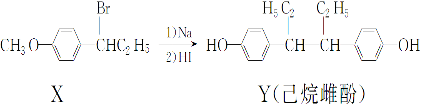
| A. | 在NaOH 水溶液中加热,化合物X 可发生消去反应 | |
| B. | 在一定条件下,化合物Y可与浓溴水发生取代反应 | |
| C. | 用FeCl3溶液不能鉴别化合物X和Y | |
| D. | 化合物Y中不含有手性碳原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 准确量取20.00mL高锰酸钾溶液,可选用25mL碱式滴定管 | |
| B. | 将水加热,Kw增大,pH不变 | |
| C. | 用惰性电极电解1L浓度均为2mol/L的AgNO3与Cu(NO3)2的混合溶液,当有0.2 mol 电子转移时,阴极析出6.4g金属 | |
| D. | NaAlO2的水溶液经加热浓缩、蒸干灼烧后能得到NaAlO2固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蒸发时将蒸发皿放置在铁架台的铁圈上,并加垫石棉网加热 | |
| B. | 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 | |
| C. | 铝箔在酒精灯火焰上加热熔化但不滴落,说明铝箔表面氧化铝膜的熔点高于铝 | |
| D. | 向某溶液中加入NaOH溶液得白色沉淀,又观察到沉淀颜色逐渐变为红褐色,说明该溶液中只含有Fe2+,不含有Mg2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3.2g氧气所含氧分子数为0.2NA | |
| B. | 1L0.1mol/L NaCl 溶液中所含的Na+为0.1NA | |
| C. | 0.012 kg 12C中含有碳原子数约为NA | |
| D. | 24g镁变成镁离子时失去的电子数为2N A |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③④⑤ | B. | ②③④ | C. | ①③④⑥ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v正(H2)=2v逆(CO) | |
| B. | 平衡常数K不再随时间而变化 | |
| C. | 混合气体的密度保持不变 | |
| D. | 混合气体的平均相对分子质量不随时间而变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该溶液可能由0.1mol/L的CH3COOH溶液与0.1mol/L的NaOH溶液等体积混合而成 | |
| B. | 该溶液可以由pH=3的CH3COOH溶液与PH=11的NaOH洛液等体积混合而成 | |
| C. | 该溶液中离子浓度的关系符合c(CH3COO-)+c (OH-)>c (Na+ )+c (H+ ) | |
| D. | 在上述溶液中加入适量NaOH,离子浓度大小可改变为:c(CH3COO-)>c (Na+ )>c (OH-)>c (H+ ) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com