
| c(OH-) |
| c(NH3?H2O) |
| c(OH-) |
| c(NH3?H2O) |


科目:高中化学 来源: 题型:
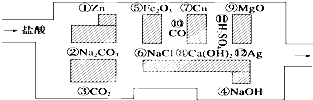
查看答案和解析>>
科目:高中化学 来源: 题型:
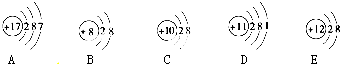
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、醋酸不小心滴到大理石桌面上,桌面失去光泽 |
| B、熏醋可一定程度上防止流行性感冒 |
| C、醋可以除去水壶上的水垢 |
| D、用醋烹饪鱼,除去鱼的腥味 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe3O4溶于足量稀HNO3:Fe3O4+8H+=Fe2++2Fe3++4H2O | ||
| B、等物质的量的MgCl2、Ba(OH)2 和 HC1 溶液混合:Mg2++2OH-=Mg(OH)2↓ | ||
| C、将过量的SO2通入Ca(ClO)2溶液中:SO2+ClO-+H2O=HClO+HSO3- | ||
D、将0.2 mol?L-1的NH4Al(SO4)2溶液与0.3 mol?L-1的Ba(OH)2溶液等体积混合:2Al3++3SO
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com