
| A. | 铅笔芯的主要成分是金属铅 | |
| B. | CO气体有毒,在生有炉火的居室中多放几盆水,可吸收CO | |
| C. | 含磷洗衣粉的大量使用会造成水体富营养化 | |
| D. | 水泥、玻璃、塑料都是高分子材料 |
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 2.20mol•L-1 | B. | 4.00mol•L-1 | C. | 5.00mol•L-1 | D. | 6.25mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 L溶液中K+浓度是0.3 mol/L | B. | 1 L溶液中含0.3NA个K+ | ||
| C. | 2 L溶液中K+浓度是1.2 mol/L | D. | 2 L溶液中含1.2NA个K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
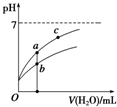 25℃时某些弱酸的电离平衡常数如下表所示:
25℃时某些弱酸的电离平衡常数如下表所示:| CH3COOH | HClO | H2CO3 |
| K(CH3COOH) =1.8×10-5 | K(HClO) =3.0×10-8 | K(H2CO3)a1=4.4×10-7 K(H2CO3)a2=4.7×10-11 |
| A. | 相同浓度的CH3COOH和HClO的混合溶液中,各离子浓度的大小关系是:c(H+)>c(ClO-)>c(CH3COO-)>c(OH-) | |
| B. | 图象中a、c两点所处的溶液中$\frac{c({R}^{-})}{c(HR)•c(O{H}^{-})}$相等(HR代表CH3COOH或HClO) | |
| C. | 图象中a点酸的浓度大于b点酸的浓度 | |
| D. | 向NaClO溶液中通入少量二氧化碳的离子方程式为:2ClO-+CO2+H2O=2HClO+CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 原子半径:r(Y)<r(Z) | |
| B. | X和Z都只能形成一种氧化物 | |
| C. | W的氧化物对应的水化物都是强酸 | |
| D. | Y的简单气态氢化物的热稳定性比W的强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯与溴水混合,水层褪色 | B. | 乙烯使溴的四氯化碳溶液褪色 | ||
| C. | 甲苯制三硝基甲苯 | D. | 苯和氢气在一定条件下生成环已烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
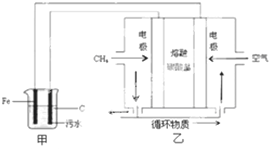
| A. | 通入空气的电极为阳极 | |
| B. | 甲装置中Fe电极的反应为Fe-3e-=Fe3+ | |
| C. | 为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时,循环物质为CO2 | |
| D. | 当乙装置中有1.6 g CH4参加反应,则C电极理论上生成气体在标准状况下为8.96 L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图.下列有关氢氧燃料电池的说法不正确的是( )
氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图.下列有关氢氧燃料电池的说法不正确的是( )| A. | 该电池中电极b是正极 | |
| B. | 外电路中电子由电极b通过导线流向电极a | |
| C. | 该电池的正极反应为O2+4H++4e-=2H2O | |
| D. | 该电池的总反应:2H2+O2=2H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com