
����Ŀ��������������Ӱ�����ǵ�����ͽ�����������Ҫ��Ⱦ��Ϊ�����������PM2.5������Ҫ��ԴΪȼú��������β���ȡ���˸�����Դ�ṹ���������ŵȴ�ʩ����Ч����PM2.5��SO2��NOx����Ⱦ����ش��������⣺
(1)��һ������ijPM2.5��Ʒ������ˮ�ܽ��Ƴɴ�������(����OH��)�������²�ø���������ɼ���Ũ�����±������ݱ��������жϸ�������pH=___________��
���� | K�� | Na�� | NH4�� | SO42�� | NO3�� | Cl�� |
Ũ��(mol��L-1) | 4��10��6 | 6��10��6 | 2��10��5 | 4��10��5 | 3��10��5 | 2��10��5 |
(2)����β����NOx��CO�����ɣ�
��֪����������NO�ķ�ӦΪ��N2(g)+O2(g) ![]() 2NO(g) ��H>0�����£������ܱ������У�����˵���У���˵���÷�Ӧ�ﵽ��ѧƽ��״̬����____��
2NO(g) ��H>0�����£������ܱ������У�����˵���У���˵���÷�Ӧ�ﵽ��ѧƽ��״̬����____��
A�����������ܶȲ��ٱ仯 B����������ѹǿ���ٱ仯
C��N2��O2��NO�����ʵ���֮��Ϊ1��1��2 D��������ת���ʲ��ٱ仯
(3)Ϊ����SO2���ŷţ���ϴ�Ӻ�SO2�����������п���Ϊϴ�Ӻ�SO2������ϴ�Ӽ��� ___________��
A��NaHCO3������Һ B��FeCl2������Һ C������CaCl2������Һ
(4)����ʹ���Ҵ����Ͳ����ܼ���NOx���ŷţ���ʹNOx����Ч������Ϊ�����������Ҫ���⡣ij�о���С����ʵ������Ag-ZSM-5Ϊ���������NOת��ΪN2��ת�������¶ȱ仯�����ͼ��ʾ������ʹ��CO���¶ȳ���775K������NO�ķֽ��ʽ��ͣ�����ܵ�ԭ��Ϊ___________________________________����n(NO)/n(CO)=1�������£�Ϊ���õij�ȥNOx���ʣ�Ӧ���Ƶ�����¶���_____K���ҡ�

(5)�����ŷŵĵ������úȼ�ղ����Ķ��������ǵ������������ġ�������ס�������̿�ɴ���������Ⱦ��NO����5L�ܱ������м���NO�ͻ���̿(����������)��һ����������������E��F�����¶ȷֱ���T1�� ��T2��ʱ����ø�����ƽ��ʱ���ʵ���(n/mol)���±���
���� �¶ȡ� | ����̿ | NO | E | F |
��ʼ | 3.000 | 0.100 | 0 | 0 |
T1 | 2.960 | 0.020 | 0.040 | 0.040 |
T2 | 2.975 | 0.050 | 0.025 | 0.025 |
��д��NO�����̿��Ӧ�Ļ�ѧ����ʽ____________________ (E,F���û�ѧʽ��ʾ)��
����T1<T2����÷�Ӧ�Ħ�H___________0��(�>����<����=��)
�ۼ���������ӦT1��ʱ��ƽ�ⳣ��K=__________________��
���𰸡�4 D A NO�ķֽ�Ϊ���ȷ�Ӧ�������¶Ȳ����ڷ�Ӧ������� 870��850-900֮�䣩 C(s)+2NO(g) ![]() CO2(g)+N2(g) < 4
CO2(g)+N2(g) < 4
��������
��1��������Һ�ʵ����ԣ���c(K��)��c(Na��)��c(NH4��)��c(H��)=2c(SO42��)��c(NO3��)��c(Cl��)��������ֵ�ó���c(H��)=10��4mol��L��1����pH=4��
��2��A����ֶ������壬�������������䣬����Ϊ����״̬������ܶȲ��䣬������Ϊ�÷�Ӧ�ﵽƽ��ı�־����A���������⣻
B����Ӧǰ������ϵ��֮����ȣ�ѹǿ֮�ȵ������ʵ���֮�ȣ����ѹǿ���䣬������Ϊ�÷�Ӧ�ﵽƽ��ı�־����B���������⣻
C����Ϊû����ʼ���ʵ�����������ж��Ƿ�ﵽƽ�⣬��C���������⣻
D��������ת���ʲ��䣬˵����Ӧ�ﵽƽ�⣬��D�������⣬��ѡD��
��3��A�������������ǿ��̼�ᣬNaHCO3��Һ������SO2����A��ȷ��
B��FeCl2��SO2��������Ӧ����˲��ܳ�ȥSO2����B���������⣻
C������CaCl2������Һ����SO2��Ӧ����˲��ܳ�ȥSO2����C���������⣬��ΪA��
��4��N2(g)��O2(g)![]() 2NO(g) ��H��0�����NO�ķֽ�Ϊ���ȷ�Ӧ�������¶ȣ������ڷ�Ӧ������У�����ͼ��870Kʱ��NO��ת���ʼ������
2NO(g) ��H��0�����NO�ķֽ�Ϊ���ȷ�Ӧ�������¶ȣ������ڷ�Ӧ������У�����ͼ��870Kʱ��NO��ת���ʼ������
��5������Ϊ�Ǵ�����Ⱦ�����NO�ͻ���̿��Ӧ��NԪ��ת����N2��Cת����CO2������Ӧ����ʽΪC(s)��2NO(g)![]() CO2(g)��N2(g)��
CO2(g)��N2(g)��
�ڸ���ͼ�����ݣ������¶�ʱ��NO�����ʵ������࣬CO2��N2�����ʵ�����С����Ӧ���淴Ӧ������У�������������ԭ��������Ӧ����Ϊ���ȷ�Ӧ������H<0��
��C(s)��2NO(g)![]() CO2(g)��N2(g)
CO2(g)��N2(g)
��ʼ�� 0.1 0 0
�仯�� 0.08 0.04 0.04
ƽ�⣺ 0.02 0.04 0.04 ���ݻ�ѧƽ�ⳣ���Ķ��壬K=![]() ��������ֵ��K=4��
��������ֵ��K=4��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����͵�����ػ������ںܶ��������Ź㷺��Ӧ�á���ش�
I.����������ʮһ�����ij���-2F���ʹ�õ��ƽ���ȼ����N��H����Ԫ����ɣ���ԭ�Ӹ���N:H=1:2����ˮ��Һ�Լ��ԡ�
(1)��������Nԭ�ӵ��ӻ���ʽΪ________������ˮ�ʼ��Ե�ԭ��Ϊ___________(�����ӷ���ʽ��ʾ)��
(2)��Ԫ�صĵ�һ�����ܱ����ڵ���Ԫ�ش���ԭ��Ϊ________________��
II.Ц��(N2O)������������������������ʳ�ᵼ������������ҡ�
(3)Ԥ��N2O�ĽṹʽΪ________________��
(4)�ڶ�����Ԫ����ɵ������У�д����NO2-��Ϊ�ȵ�����ķ���_________��(д�����������ʽ)
III.������Ϊ���ɫ���壬�з½�Ч����Խ��Խ��س�Ϊ�ƽ�Ĵ���Ʒ��
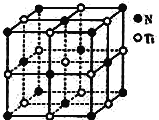
(5)Ti��������Ķѻ�ģ��Ϊ________����λ��Ϊ_______����̬Ti3+��δ�ɶԵ�������______����
(6)�����Ѿ���ľ�����NaCl��������(��ͼ��ʾ)���õ����ѵ��ܶ�Ϊ��g��cm-3����þ�����N��Ti֮����������Ϊ______nm(NAΪ�����ӵ�������ֵ��ֻ�м���ʽ)���þ������뵪ԭ�Ӿ���������������ԭ��Χ�ɵĿռ伸����Ϊ____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȼ��ʱ�������仯ͼ���ж��й��Ȼ�ѧ����ʽ��˵����ȷ����(����)

A. S(s����б)��O2(g)===SO2(g) ��H����297.16 kJ��mol��1
B. S(s������)===S(s����б)����H����0.33 kJ��mol��1
C. S(s������)��O2(g)===SO2(g)����H����296.83 kJ��mol��1
D. ��б����ȶ��Դ�����������ȶ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�����л�ԭ��A�Ʊ� �;�������ϩ����������Ϊ��
�;�������ϩ����������Ϊ��

��֪����![]() ��
��![]()
��ش��������⣺
��1��A��B�ķ�Ӧ������___________��J�й����ŵ�����Ϊ___________��
��2����Ӧ�ڵ��Լ��������ֱ���___________��G�Ľṹ��ʽ��___________��
��3��д����Ӧ�ٵĻ�ѧ����ʽ��_________________________________��
��4����A������ͬ��������ֻ��һ�����ķ��㻯�����ͬ���칹���ж��֣�д������һ�ֺ˴Ź�������Ϊ��������ܷ���������Ӧ�Ľṹ��ʽΪ______________________��
��5����������ʾ���ϳ�·�ߣ����һ�����Ҷ���Ϊ��ʼԭ���Ʊ����Ҷ����Ҷ��ĺϳ�·�ߡ�ʾ����![]() _______________
_______________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ��װ�ý�����Ӧʵ�飬�ܴﵽʵ��Ŀ���ǣ� ��
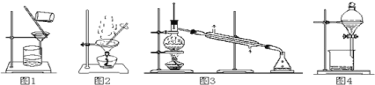
����ͼ1��ʾװ�ô�Fe(OH)3�����й��˳�Fe(OH)3����
����ͼ2��ʾװ�ô��Ȼ�����Һ�еõ��Ȼ��ƾ���
����ͼ3��ʾװ�ôӵ�����Ȼ�̼��Һ�з�������Ȼ�̼
����ͼ4��ʾװ�ô��Ҵ��뱽�Ļ�����з������
A.�٢�B.�ڢ�C.�ڢۢ�D.�٢ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)д��NaHSO4��ˮ�еĵ��뷽��ʽ________��
(2)�����к�������CaCl2��MgCl2��һЩ�����Σ�Ҫ��ȥ��Щ���ʣ���ѡ�������Լ�����Na2CO3����NaOH����BaCl2����HCl �����Լ�������Ⱥ�˳����__________(�����)��
(3)2KMnO4+16HCl(Ũ) =2KCl+2MnCl2+5Cl2��+8H2O����˫���ŷ�����÷�Ӧ����ת�Ƶķ������Ŀ_______������0.1mol����ת��ʱ����Cl2�����Ϊ__________(��״��)����������HCl�����ʵ���Ϊ______________��
(4)ij��ɫ����Һ���ܺ���K+��Cu2+��Ca2+��SO42-��CO32-��Cl���еļ��֣��ֽ�������ʵ�飺
�ٵμ�BaCl2��Һ���а�ɫ�����������������˳���
�������������м���������ϡ���ᣬ�в��ֳ����ܽ⡣
������Һ����AgNO3��Һ���а�ɫ�������ɣ��ó���������ϡHNO3��
���жϣ�����Һ�п϶���__________���϶�û��_________��������_________�������ӷ��ţ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵��������ˮ���й�����ȷ����: ( )
A. AlCl3��Һ��NaAlO2��Һ���ȡ�������Ũ�����ᾧ�����գ����ù���ijɷ���ͬ
B. ����FeCl3��Һʱ����FeCl3�����ܽ��������У�Ȼ������ˮϡ�͵������Ũ��
C. �ü��ȵķ����ɳ�ȥKCl��Һ�л��е�Fe3��
D. ʳ�����ܽ�ˮ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������A��B��C��D����Ԫ�أ���֪AԪ���ǵؿ��к�������Ԫ�أ�BԪ��Ϊ����Ԫ�أ�����ԭ�Ӻ���K��L���ϵ�����֮�͵���M��N�������֮�ͣ�CԪ���ǵ������ڵ�һ��������С��Ԫ�أ�DԪ���ڵ��������е縺�����
��1�����ƶ�A��B��C��D����Ԫ�صķ��ţ�A________��B________��C________��D________��
��2��д��AԪ��ԭ�ӵĺ�������Ų�ʽ��____________��д��BԪ��ԭ�Ӻ�������Ų��ļ۵��ӹ��ͣ�__________���õ����Ų�ͼ��ʾCԭ�ӵĺ�������Ų������_______________��
��3���Ƚ�����Ԫ�صĵ�һ�����ܺ͵縺�ԵĴ�С����һ������____________���縺��____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪N2O4(��ɫ)![]() 2NO2(����ɫ) ��������ͼ��ʾ��������ƿ,�ֱ����NO2���岢�ֱ������ʢ���������ʵ��ձ�(�ձ�����ˮ)�У�����I���м�����ˮCaO������III���м���NH4Cl���壬��II���в��������κ����ʣ�������I���к���ɫ�����III���к���ɫ��dz������������ȷ���� (�� ��)
2NO2(����ɫ) ��������ͼ��ʾ��������ƿ,�ֱ����NO2���岢�ֱ������ʢ���������ʵ��ձ�(�ձ�����ˮ)�У�����I���м�����ˮCaO������III���м���NH4Cl���壬��II���в��������κ����ʣ�������I���к���ɫ�����III���к���ɫ��dz������������ȷ���� (�� ��)

A. CaO����ˮʱ�������� B. �÷�Ӧ����H>0
C. NH4Cl����ˮʱ�ų����� D. ��ƿ(III)�������ѹǿ����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com