
某同学对“CO2是共价化合物和NH4Cl是离子化合物”有下列感悟, 其中不正确的是( )
A.离子化合物中可能含共价键
B.共价化合物中一定不含离子键
C.所有物质中都含有化学键
D.离子化合物中不一定含金属元素
科目:高中化学 来源:2013-2014山东省日照市高三5月二模理综化学试卷(解析版) 题型:推断题
醇酸树脂是一种成膜性好的树脂,下面是一种醇酸树脂的合成线路:

(1)B中含有的官能团的名称是_________________________。
(2)反应①、③的有机反应类型分别是___________________、____________________。
(3)下列说法正确的是__________(填字母编号)。
a.1 mol E与足量的银氨溶液反应能生成2mol Ag
b.F能与NaHCO3反应产生CO2
c.检验CH3CH2CH2Br中的溴原子时,所加试剂的顺序依次是过量氢氧化钠溶液、硝酸银溶液
(4)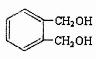 的同分异构体中同时符合下列条件的芳香族化合物共有__________种。
的同分异构体中同时符合下列条件的芳香族化合物共有__________种。
a.能发生消去反应 b.能与过量浓溴水反应生成白色沉淀
(5)写出反应⑤的化学方程式________________________________________________
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省兰陵县下学期期中考试高二化学试卷(解析版) 题型:选择题
下列物质属于芳香烃,但不是苯的同系物的是( )
①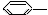 CH3 ②
CH3 ②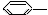 CH=CH2 ③
CH=CH2 ③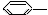 NO2
NO2
④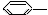 OH ⑤
OH ⑤ 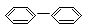 ⑥
⑥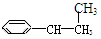
A.③④ B.②⑤ C.①②⑤⑥ D.②③④⑤⑥
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省兰陵县下学期期中考试高一化学试卷(解析版) 题型:选择题
下图是可逆反应X2 + 3Y2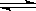 2Z2 在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是( )。
2Z2 在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是( )。
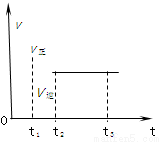
A.t1时,只有正方向反应
B. t2- t3,各物质的浓度不再发生变化
C.t2- t3,反应不再发生
D.t2时,反应未到达限度
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省兰陵县下学期期中考试高一化学试卷(解析版) 题型:选择题
下列反应前后物质的总能量变化能用下图表示的是( )
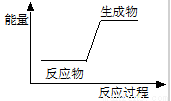
A.生石灰和水的反应
B.石灰石在高温下的分解反应
C.盐酸与氢氧化钠溶液的反应
D.木炭在氧气中燃烧
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省乳山市下学期期中考试高一化学试卷(解析版) 题型:简答题
(13分)有A、B、C、D、 E、R六种短周期元素,其元素特征信息如下表:
E、R六种短周期元素,其元素特征信息如下表:
元素编号 | 元素特征信息 |
A | 其单质是密度最小的物质 |
B | 其阴离子带两个单位的负电荷,单质是空气主要成分之一 |
C | 其阳离子与B的阴离子具有相同的电子层结构,其原子的最外层电子数是次外层的1/4 |
D | 其氢氧化物和氧化物都有两性,且与C同周期 |
E | 与C同周期,其原子半径在该周期最小 |
R | 有多种化合价,其最高正价为+6价 |
回答下列问题:
(1)写出下列元素的名称:C ,E ;画出B的阴离子结构示意图: 。
(2)B、C、D的简单离子半径由大到小的顺序是 (用化学式表示)。E元素的最高价含氧酸的化学式是 ;
(3)实验证明D的氢氧化物(或氧化物)具有两性的操作方法是: 。
(4)在一定条件下,RO32-与R2-可发生反应:RO32-+2R2-+6H+ = 3R+3H2O,下列有关叙述中,正确的是 (填序号)。
A.元素R位于周期表中第3 周期,ⅥA族
B.R2-与氖原子电子层结构相同
C.RO32-在它能发生的所有反应中都只具有氧化性
D.反应中消耗1 mol RO32- ,转移的电子的物质的量为4 mol
(5)请写出涉及上述元素间的两个反应的离子方程式,要求:(1)单质之间的置换 (2)在方程式中如为两种非金属则必须是不同主族的。 ; 。
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省乳山市下学期期中考试高一化学试卷(解析版) 题型:选择题
已知某反应的能量变化如图所 示,下列说法正确的是
示,下列说法正确的是

A.该反应可用于表示烧碱与硫酸反应
B.该反应只有在加热条件下才能进行
C.反应物的总能量高于生成物的总能量
D.该反应可用于表示碳酸钙受热分解的反应
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省临沂市高三三模试卷理科综合化学试卷(解析版) 题型:填空题
(17分)运用化学反应原理研究碳的化合物具有重要意义。
(1)常温下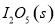 可用于检测CO,反应原理为:
可用于检测CO,反应原理为: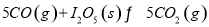
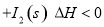 。向2L密闭容器中加入足量
。向2L密闭容器中加入足量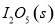 ,并通人1molCO,CO2的体积分数
,并通人1molCO,CO2的体积分数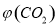 随时间的变化如下图所示。
随时间的变化如下图所示。
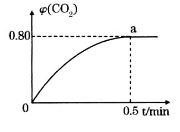
①0~0.5min内的平均反应速率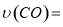 _____________。
_____________。
②保持温度和体积不变,若开始加入CO(g)的物质的量是原来的2倍,则下列说法正确的是____________(填代号)。
a.生成I2的质量为原来的2倍
b.混合气体的平均摩尔质量不变
c.达到平衡的时间为原来的2倍
d.混合气体的密度不变
③反应达a点时,欲增大容器中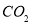 的体积分数
的体积分数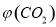 ,可采取的措施为____________。
,可采取的措施为____________。
(2)以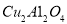 为催化剂,可以将
为催化剂,可以将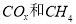 的混合气体直接转化为乙酸。
的混合气体直接转化为乙酸。
①若该反应的原子利用率为100%,则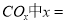 ______________。
______________。
②在25℃下,将pH=a的氢氧化钠溶液与pH=b的醋酸溶液等体积混合,若两溶液恰好完全反应,则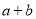 ________14(填“>”、“<”或“=”);该温度下醋酸的电离常数K=__________(用含a、b的式子表示)。
________14(填“>”、“<”或“=”);该温度下醋酸的电离常数K=__________(用含a、b的式子表示)。
(3)利用反应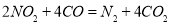 可以处理汽车尾气,若将该反应设计为原电池,用熔融Na2O作电解质,其正极电极反应式为________________________________。
可以处理汽车尾气,若将该反应设计为原电池,用熔融Na2O作电解质,其正极电极反应式为________________________________。
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省东营市高三第二次模拟理科综合化学试卷(解析版) 题型:简答题
(12分)【化学-物质结构与性质】
原子序数依次增大的A、B、C、D、E、F六种元素。其中A的基态原子有3个不同的能级,各能级中的电子数相等;C的基态原子2p能级上的未成对电子数与A原子的相同;D为它所在周期中原子半径最大的主族元素;E和C位于同一主族,F的原子序数为29。
(1)F原子基态的核外电子排布式为 。
(2)在A、B、C三种元素中,第一电离能由小到大的顺序是 (用元素符号回答)。
(3)元素B的简单气态氢化物的沸点远高于元素A的简单气态氢化物的沸点,其主要原因是 。
(4)由A、B、C形成的离子CAB-与AC2互为等电子体,则CAB-的结构式为 。
(5)在元素A与E所形成的常见化合物中,A原子轨道的杂化类型为 。
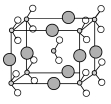
(6)由B、C、D三种元素形成的化合物晶体的晶胞如图所示,则该化合物的化学式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com