
如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
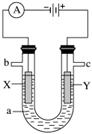
(1)若X、Y是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞,则:
①电解池中X极上的电极反应式是____________________________________________,
在X极附近观察到的现象是_________________________________________________。
②Y电极上的电极反应式是_______________________________________,
检验该电极反应产物的方法是____________________________________________。
(2)若用电解方法精炼粗铜,电解液a选用CuSO4溶液,则:
①X电极的材料是________________________________________,
电极反应式是__________________________________________。
②Y电极的材料是__________________________________________,
电极反应式是________________________________________________
(说明:杂质发生的电极反应不必写出)。
③当电路中有0.04 mol电子通过时,阴极增重_____________________________ g。
答案 (1)①2H++2e-===H2↑ 有气泡产生,溶液变红色 ②2Cl--2e-===Cl2↑ 将湿润的KI淀粉试纸置于c口处,试纸变蓝
(2)①纯铜 Cu2++2e-===Cu ②粗铜 Cu-2e-===Cu2+ ③1.28
解析 (1)①电解池中X极是阴极,发生还原反应,电极反应式为2H++2e-===H2↑,可以看到电极上有气泡产生,且由于H+放电使X极附近溶液中OH-浓度增大,使酚酞溶液变红色。②Y电极上是Cl-放电,电极反应式为2Cl--2e-===Cl2↑。(2)电解精炼粗铜,阳极用粗铜,阴极用纯铜。根据反应,电路中通过2 mol电子,阴极析出1 mol铜,故当电路中通过0.04 mol电子时,析出0.02 mol Cu,阴极增重1.28 g。


 作业辅导系列答案
作业辅导系列答案 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案科目:高中化学 来源: 题型:
500 mL KNO3和Cu(NO3)2的混合溶液中c(NO )=0.6 mol·L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到2.24 L气体(标准状况下),假定电解后溶液体积仍为500 mL,下列说法正确的是( )
)=0.6 mol·L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到2.24 L气体(标准状况下),假定电解后溶液体积仍为500 mL,下列说法正确的是( )
A.原混合溶液中c(K+)为0.2 mol·L-1
B.上述电解过程中共转移0.2 mol电子
C.电解得到的Cu的物质的量为0.05 mol
D.电解后溶液中c(H+)为0.2 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究小组为探究弱酸性条件下铁发生电化学腐蚀类型的影响因素,将混合均匀的新制铁粉和碳粉置于锥形瓶底部,塞上瓶塞(如图1)。从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化。
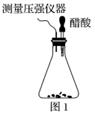
(1)请完成以下实验设计表(表中不要留空格):
| 编号 | 实验目的 | 碳粉/g | 铁粉/g | 醋酸/% |
| ① | 为以下实验作参照 | 0.5 | 2.0 | 90.0 |
| ② | 醋酸浓度的影响 | 0.5 | 36.0 | |
| ③ | 0.2 | 2.0 | 90.0 |
(2)编号①实验测得容器中压强随时间变化如图2。t2时,容器中压强明显小于起始压强,其原因是铁发生了________腐蚀,请在图3中用箭头标出发生该腐蚀时电子流动方向;此时,碳粉表面发生了________(填“氧化”或“还原”)反应,其电极反应式是________________。

(3)该小组对图2中0~t1时压强变大的原因提出了如下假设,请你完成假设二:
假设一:发生析氢腐蚀产生了气体;
假设二:________________________________________________________________________;
……
(4)为验证假设一,某同学设计了检验收集的气体中是否含有H2的方案。请你再设计一个实验方案验证假设一,写出实验步骤和结论。
| 实验步骤和结论(不要求写具体操作过程): |
查看答案和解析>>
科目:高中化学 来源: 题型:
用石墨电极电解100 mL H2SO4与CuSO4的混合溶液,通电一段时间后,阴、阳两极分别收集到2.24 L和3.36 L气体(标准状况),溶液要想恢复电解前的状态可加入下列( )
A.0.1 mol CuO
B.0.1 mol CuCO3
C.0.1 mol Cu(OH)2
D.0.1 mol Cu2(OH)2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
某反应的ΔH=+100 kJ·mol-1,下列有关该反应的叙述正确的是( )
A.正反应活化能小于100 kJ·mol-1
B.逆反应活化能一定小于100 kJ·mol-1
C.正反应活化能不小于100 kJ·mol-1
D.正反应活化能比逆反应活化能大100 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
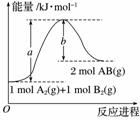
已知化学反应A2(g)+B2(g)===2AB(g)的能量变化如图所示,请写出该反应的热化学方程式:________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
判断正误,正确的划“√”,错误的划“×”
(1)太阳能是清洁能源( )
(2)化石燃料和植物燃料燃烧时放出的能量均来源于太阳能( )
(3)农村用沼气池产生的沼气作燃料属于生物质能的利用( )
(4)人类利用的能源都是通过化学反应获得的( )
(5)随着科技的发展,氢气将成为主要能源之一( )
(6)食用植物体内的淀粉、蛋白质等属于直接利用能源( )
(7)粮食作物是制乙醇燃料的重要原料( )
(8)化石燃料属于可再生能源,不影响可持续发展( )
(9)开发利用各种新能源,减少对化石燃料的依赖,可以降低空气中PM2.5的含量( )
(10)开发太阳能、水能、风能、可燃冰等新能源,减少使用煤、石油等化石燃料( )
(11)低碳生活注重节能减排,尽量使用太阳能等代替化石燃料,减少温室气体的排放( )
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com