
【题目】(1)MnO2的生产方法之一是以石墨为电极,电解酸化的MnSO4溶液。阴极的电极反应式是______________。若电解电路中通过2mol电子,MnO2的理论产量为______ 克。
(2)高铁酸钠生产方法之一是电解法,其原理为Fe+2NaOH+2H2O![]() Na2FeO4+3H2↑,则电解时阳极的电极反应式是_____________________。
Na2FeO4+3H2↑,则电解时阳极的电极反应式是_____________________。
(3)用惰性电极电解100ml4mol/L的Cu(NO3)2溶液,一段时间后在阳极收集到标况下气体1.12L,
停止电解,向电解后的溶液中加入足量的铁粉,充分作用后溶液中Fe2+浓度为(设溶液体积不
变)_______________。
【答案】 2H++2e-=H2↑ 87g Fe+8OH――6e-=FeO42-+4H2O 3.75mol/L
【解析】(1)电解时阴极连接电源的负极,肯定是提供电子的,所以阴极发生的反应是得电子的反应,能够得电子的要么是不活泼金属阳离子,要么是H+(酸性溶液中),要么是水(中性或碱性溶液中),然后看溶液中有哪些可以得电子:Mn2+、H+、H2O三种,Mn比H活泼,又在酸性溶液中,所以得电子的是H+.反应为:2H+ + 2e ![]() H2;Mn2+ → MnO2,需要失去2个电子,所以电路中通过2mol电子,MnO2的理论产量是1mol,即87g;(附:阳极反应为:Mn2+ + 2H2O - 2e
H2;Mn2+ → MnO2,需要失去2个电子,所以电路中通过2mol电子,MnO2的理论产量是1mol,即87g;(附:阳极反应为:Mn2+ + 2H2O - 2e ![]() MnO2 + 4H+)
MnO2 + 4H+)
(2)Fe+2NaOH+2H2O![]() Na2FeO4+3H2↑中Fe是还原剂,失电子,故电解时阳极的电极反应式是Fe+8OH――6e-=FeO42-+4H2O ;
Na2FeO4+3H2↑中Fe是还原剂,失电子,故电解时阳极的电极反应式是Fe+8OH――6e-=FeO42-+4H2O ;
(3)1.12÷22.4=0.05mol
2Cu(NO3)2+2H2O ![]() 2Cu↓+O2↑+4HNO3
2Cu↓+O2↑+4HNO3
2mol 1mol 4mol
x 0.05mol y
x=0.1mol y=0.2mol
溶液中含有0.4-0.1=0.3mol的Cu(NO3)2和0.2mol的HNO3
所以 8HNO3+3Fe![]() =3Fe(NO3)2+2NO↑+4H2O
=3Fe(NO3)2+2NO↑+4H2O
8mol 3mol
0.2mol a
a=0.075mol
Fe+Cu2+=Fe2++Cu
1 1
0.3mol b
b=0.3mol
所以Fe2+的浓度为c=3.75mol·L-1


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列离子或分子在溶液中能大量共存的是
A. K+、OH-、H+、NO3-
B. Na+、Ca2+、CO32-
C. Na+、SO42-、Cl-
D. Al3+、NO3-、NH3·H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是一种正在投入生产的大型蓄电池系统的原理图,电池中的左右两侧为电极,中间为钠离子选择性膜(电池放电和充电时该膜只允许钠离子通过),电池充、放电时反应的化学方程式为2Na2S2+NaBr2![]() Na2S4+3NaBr。下列关于此电池的说法错误的是
Na2S4+3NaBr。下列关于此电池的说法错误的是

A. 电极a接触到的电解质溶液为Na2S2-Na2S4混合溶液
B. 放电过程中,钠离子从电极b通过钠离子选择性膜移动到电极a
C. 电池放电时,负极的电极反应式为3Br--2e-=Br3-
D. 充电过程中,当有0.1molNa+通过钠离子选择性膜时,导线中通过0.2mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新装修房屋会释放有毒的甲醛(HCHO)气体,银-Ferrozine法检测甲醛的原理如下:

下列说法正确的是
A. 22.4LCO2中含共价键数目为4NA
B. 30gHCHO被氧化时转移电子数目为2 NA
C. 该电池总反应的化学方程式为2Ag2O+HCHO=4Ag+CO2↑+H2O
D. 理论上,消耗HCHO和消耗Fe3+的物质的量之比4:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于甲、乙、丙、丁四种有机物说法正确的是( )

A. 甲、乙、丙、丁中加入NaOH的醇溶液共热,然后加入稀硝酸呈酸性,再滴入AgNO3溶液,均有沉淀生成
B. 甲中加入NaOH的水溶液共热,再滴入AgNO3溶液,可检验该物质中含有的卤素原子
C. 乙发生消去反应得到两种烯烃
D. 丙与NaOH的水溶液共热,反应后生成的醇能被氧化为醛
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.A~D是四种烃分子的球棍模型(如图)

(1)与A互为同系物的是___________(填序号)
(2)能使酸性高锰酸钾溶液褪色的物质是_____________(填序号)
(3)D和液溴反应的化学方程式是___________________________
Ⅱ.某些有机物的转化如下图所示。已知:A是营养物质之一,米饭、馒头中富含A,在酸性条件下水解的最终产物是B。C是白酒的主要成分,能直接氧化成酸性物质D。
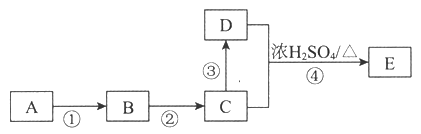
请回答下列问题:
(1)A的名称是_____________;C中官能团的名称是__________
(2)反应③所需要的试剂是__________________
(3)反应④的化学方程式是__________________________
(4)若实验室利用下图制备E,导管口不能深入N试管中液面下的原因是_______________

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】塑化剂主要用作塑料的增塑剂,也可作为农药载体、驱虫剂和化妆品等的原料。添加塑化剂(DBP)可改善白酒等饮料的口感,但超过规定的限量会对人体产生伤害。其合成线路图如图I所示:

已知以下信息:
①
②R1CHO + R2CH2CHO![]()
 +H2O(—R1、—R2表示氢原子或烃基)
+H2O(—R1、—R2表示氢原子或烃基)
③其中A的化学式是C8H10;C为含两个碳原子的烃的含氧衍生物,其核磁共振氢谱图如图II所示:峰的强度之比为2:1:3
请根据以上信息回答下列问题:
(1)C的结构简式为______, E中所含官能团的名称是_____________;
(2)写出下列有关反应的化学方程式:
①E和H2以物质的量比1︰1反应生成F:_______________________;
②B和F以物质的量比1︰2合成DBP:_______________________________,该反应的反应类型为__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物W (分子式C3H6O3)能与NaHCO3反应,分子中含有四种活动性不同的氢原子,个数比为3 : 1 : 1 :1。
(1)W的结构简式是______________________________。
(2)W在不同条件下可脱水形成不同物质,写出W形成高分子化合物一聚酯的反应方程式_______________________________。
(3)W的工业合成路线如下图所示:

己知:I A、B、C、D与W分子中含有相同碳原子数;
II ![]()
①写出A的名称__________________。
②B与新制Cu(OH)2反应的化学方程式是____________________________。
③某有机物与C互为同分异构体,既属于酯类,又含醛基。则该有机物可能的结构简式为______________________________。
④W的某种同分异构体具有下列性质:能发生银镜反应;1mol该物质能跟金属钠反应产生1molH2,则该同分异构体的结构简式为_____________________(己知同一个碳原子上不能连接2个羟基)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关元素周期表和元素周期律的说法,错误的是
①元素周期表中s区、d区和ds区的元素都是金属元素
②d区元素最后一个核外电子一定填充在s能级上
③原子核外电子的能层越多,原子半径越大
④同一周期自左至右,元素的第一电离能依次增大
A. 只有①②③ B. 只有②③ C. 只有③④ D. ①②③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com