
【题目】已知某气体反应的平衡常数可表示为K=c(CH3OCH3)c(H2O)/[c(CH3OH)]2 , 该反应在不同温度下的平衡常数:400℃,K=32;500℃,K=44.
请回答下列问题:
(1)写出上述反应的化学方程式
(2)该反应的正反应是反应(填“放热”或者“吸热”),
(3)已知在密闭容器中,测得某时刻各组分的浓度如下:
物质 | CH3OH(g) | CH3OCH3(g) | H2O(g) |
浓度/(molL﹣1) | 0.54 | 0.68 | 0.68 |
①此时系统温度400℃,比较正、逆反应速率的大小:v正v逆 (填“>”、“<”或“=”).
②若以甲醇百分含量为纵坐标,以温度为横坐标,此时反应点在图象的位置是图中点.比较图中B、D两点所对应的正反应速率BD(填“>”、“<”或“=”).理由是 . 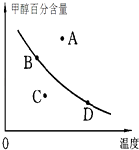
(4)一定条件下要提高反应物的转化率,可以采用的措施是
a.升高温度 b.加入催化剂 c.压缩容器的体积
d.增加水蒸气的浓度 e.及时分离出产物.
【答案】
(1)2CH3OH(g) ![]() CH3OCH3(g)+H2O(g)
CH3OCH3(g)+H2O(g)
(2)吸热
(3)>;A;<;D点温度高于B点,温度越高反应速率越大,所以反应速率也大于B
(4)ae
【解析】解:(1)由平衡常数的表达式:K= ![]() ,可知该反应的反应物为甲醇,生成物为二甲醚和水;化学方程式为2CH3OH(g)
,可知该反应的反应物为甲醇,生成物为二甲醚和水;化学方程式为2CH3OH(g) ![]() CH3OCH3(g)+H2O(g);(2)该反应在不同温度下的平衡常数:400℃,K=32;500℃,K=44,温度升高,平衡常数增大,说明温度升高,平衡向正反应方向移动,又升高温度,平衡向吸热反应方向移动,所以正反应为吸热反应;(3)①此时浓度商Q=
CH3OCH3(g)+H2O(g);(2)该反应在不同温度下的平衡常数:400℃,K=32;500℃,K=44,温度升高,平衡常数增大,说明温度升高,平衡向正反应方向移动,又升高温度,平衡向吸热反应方向移动,所以正反应为吸热反应;(3)①此时浓度商Q= ![]() =1.55<32,反应未达到平衡状态,向正反应方向移动,故v正> v逆;
=1.55<32,反应未达到平衡状态,向正反应方向移动,故v正> v逆;
②由①可知平衡向正反应方向移动,所以甲醇的百分含量大于平衡时的含量,此时反应点应在A点;根据影响化学反应速率的因素,温度越高反应速率越大,D点温度高于B点,所以D点对应的正反应速率也大于B点;(4)a、正反应是吸热反应,升高温度平衡向正反应方向移动,甲醇的平衡浓度减小,转化率增大;
b、加入催化剂,平衡不移动,转化率不变;
c、该反应为体积不变的反应,压缩容器体积,平衡不移动,转化率不变;
d、增加水蒸气浓度,平衡向逆反应方向移动,甲醇的转化率减小;
e、及时分离产物,平衡向正反应方向移动,甲醇的转化率增大;
故选ae.
所以答案是:(1)2CH3OH(g) ![]() CH3OCH3(g)+H2O(g); (2)吸热;(3)①>;
CH3OCH3(g)+H2O(g); (2)吸热;(3)①>;
②A,<,D点温度高于B点,温度越高反应速率越大,所以反应速率也大于B;(4)ae
【考点精析】根据题目的已知条件,利用化学平衡常数的含义和化学平衡状态本质及特征的相关知识可以得到问题的答案,需要掌握指在一定条件下的可逆反应里,正反应和逆反应的速率相等,反应混合物中各组分的浓度不变的状态;化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效).


科目:高中化学 来源: 题型:
【题目】回答下问题:
(1)下列说法不正确的是(填字母序号).
A.铝的氧化物属于碱性氧化物
B.光纤制品的基本原料为SiO2
C.用热的纯碱溶液洗涤沾有油污的器具时发生的主要是化学变化
D.液氨、液氯、液态氯化氢都是非电解质
E.丁达尔效应可用于区别溶液与胶体,云、雾均能产生丁达尔效应
F.化学变化前后原子的种类、数目不变,分子数目也不变
(2)出土的青铜器大多受到魂晶腐蚀,某青铜器中Sn、Pb的质量分别为119g、20.7g,则该青铜器中Sn和Pb原子的数目之比为采用“局部封闭法”可以防止青铜器进一步被腐蚀.如将糊状Ag2O涂在被腐蚀部位,Ag2O与有害组分CuCl发生复分解反应,该化学方程式为
(3)KNO3中NO3﹣的空间构型为 , 写出与NO3﹣互为等电子体的另一种阴离子的化学式:
(4)已知配合物CrCl36H2O中心原子Cr3+配位数为6,向含0.1molCrCl36H2O的溶液中滴加2mol/LAgNO3溶液,反应完全后共消耗AgNO3溶液50mL,则该配离子的化学式为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.0.1mol/LCH3COOH溶液加水稀释,溶液中c(OH﹣)增大
B.将NaOH和氨水溶液各稀释一倍,两者的OH﹣浓度均减少到原来的 ![]()
C.相同浓度的HCl和CH3COOH,两溶液中c(H+)相同
D.甲溶液的pH是5,乙溶液的pH是4,则甲溶液与乙溶液的中c(H+)之比为10:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下向10mL pH=3的醋酸溶液中加水稀释后,下列说法正确的是( )
A.溶液中导电粒子的数目减少
B.溶液中 ![]() 值减小
值减小
C.醋酸的电离程度增大,c(H+)亦增大
D.再加入10mL pH=11的NaOH溶液,混合液pH=7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组热化学方程式中,化学反应的△H前者大于后者的是( )
①C(s)+O2(g)═CO2(g);△H1 C(s)+ ![]() O2(g)═CO(g);△H2
O2(g)═CO(g);△H2
②S(s)+O2(g)═SO2(g);△H3 S(g)+O2(g)═SO2(g);△H4
③H2(g)+ ![]() O2(g)═H2O(l);△H5 2H2(g)+O2(g)═2H2O(l);△H6
O2(g)═H2O(l);△H5 2H2(g)+O2(g)═2H2O(l);△H6
④CaCO3(s)═CaO(s)+CO2(g);△H7 CaO(s)+H2O(l)═Ca(OH)2(s);△H8 .
A.①
B.④
C.②③④
D.①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究性学习小组进行了一系列化学实验后,发现高锰酸钾分解后的含锰元素的化合物都能和浓盐酸反应制得氯气,且锰化合物的还原产物都是MnCl2 . 他们将6.32gKMnO4粉末加热一段时间,也不知道高锰酸钾是否完全分解,收集到0.112L气体后便停止加热了,冷却后放入足量的浓盐酸再加热,又收集到气体体积是(上述气体体积都折合成标准状况)( )
A.0.448L
B.2.240L
C.2.016L
D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(双选题)关于Al2O3下列说法正确的是( )
A.Al2O3可以通过分解反应和化合反应制得
B.Al2O3是两性氧化物
C.Al2O3薄膜非常致密,所以可用铝制容器盛放HCl溶液和NaOH溶液等
D.擦去表面氧化铝的铝条,在酒精灯上灼烧时,熔化的铝纷纷滴落下来
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.已知HClO是比H2CO3还弱的酸,HClO的电离平衡常数为2.95×10-5,H2CO3的电离平衡常数为K1=4.3×10-7和K2=5.6×10-11氯水中存在下列平衡:Cl2+H2O![]() HCl+HClO,HClO
HCl+HClO,HClO![]() H++ClO-,达平衡后
H++ClO-,达平衡后
(1)要使HClO浓度增加,可加入下列物质________(填代号)。
A.SO2 B.NaHCO3 C.HCl D.NaOH
(2)由此说明在实验室可用排饱和食盐水收集Cl2的理由是________________。
Ⅱ.Al(OH)3的电离方程式可表示为:H2O+AlO2-+H+![]() Al(OH)3
Al(OH)3![]() Al3++3OH-。
Al3++3OH-。
试根据平衡移动原理,解释下列有关问题。
(1)向Al(OH)3沉淀中加入盐酸,沉淀溶解,其原因是_________________,有关离子方程式为__________________。
(2)向Al(OH)3沉淀中加入苛性钠溶液,沉淀溶解,其原因是________________,有关离子方程式为__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com