
A.某溶液中加入铝片有氢气产生,则在该溶液中一定能大量共存的离子是:Cl-、![]() 、Ba2+、Mg2+
、Ba2+、Mg2+
B.某金属硝酸盐受热分解生成金属氧化物、二氧化氮和氧气。若生成的二氧化氮和氧气的物质的量之比为8∶1,则金属元素的化合价在反应过程中的变化是升高
C.从有机物分类看,对氨基苯甲酸丁酯可属于“氨基酸类”“酯类”“芳香烃类”
D.在稀溶液中,H+(aq)+OH-(aq)====H2O(l);ΔH=-57.3 kJ·mol-1,若将含0.5 mol H2SO4的浓硫酸(98%)与含1 mol NaOH的浓溶液混合,放出的热量大于57.3 kJ
科目:高中化学 来源: 题型:
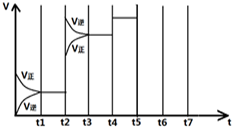 在一定条件下发生化学反应:2SO2(g)+O2(g)?2SO3(g)△H=-197kJ/mol.现有容积均为1L的甲、乙两个容器,在上述条件下分别充入气体,到达平衡时,反应放出的热(Q),及平衡时的转化率(X)如下表所示:
在一定条件下发生化学反应:2SO2(g)+O2(g)?2SO3(g)△H=-197kJ/mol.现有容积均为1L的甲、乙两个容器,在上述条件下分别充入气体,到达平衡时,反应放出的热(Q),及平衡时的转化率(X)如下表所示:| 容器 | 起始时各物质的量 | 到达平衡时放出的热量(QkJ) | 平衡时SO2转化率 (X) | |||
| SO2 | O2 | SO3 | N2 | |||
| 甲 | 2 | 1 | 0 | 0 | Q1 | X1 |
| 乙 | 1 | 0.5 | 0 | 1 | Q2= 39.4 |
X2 |
| t 1-t 2 | t 3-t 4 | t 4-t 5 | t 6-t 7 |
| K1 | K2 | K3 | K4 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源:2013届江西省上饶市高一下学期期中考试化学试卷 题型:选择题
下列说法错误的是
A.在C(s) +H2O(g)  CO(g) + H2(g)反应体系中,增加碳的量不能迅速提高正反应速率
CO(g) + H2(g)反应体系中,增加碳的量不能迅速提高正反应速率
B.钾的金属性比钠强,所以钾与水的反应比钠的反应剧烈
C.在压强相同条件下,结构相似的CH4、SiH4、GeH4的沸点依次升高,所以结构相似的HF、HCl、HBr、HI的沸点也依次升高
D.面粉厂严禁烟火的原因是面粉粉尘表面积大,与空气接触遇明火极易发生爆炸
查看答案和解析>>
科目:高中化学 来源:2013届江苏省盐城市高一下学期期中考试化学试卷 题型:选择题
氢氧燃料电池已用于航天飞机。以30%KOH溶液为电解质溶液的这种电池在使用时的电极反应如下:2H2+4OH—-4e—=4H2O,2H2O+O2+4e—==4OH—。
据此判断,下列说法错误的是
A.H2在负极发生氧化反应 B.供电时总反应为:2H2+ O2==2H2O
C.燃料电池的能量转化率为100% D.产物为无污染的水,属环境友好电池
查看答案和解析>>
科目:高中化学 来源:2013届广东省高一上学期期末考试化学试卷 题型:选择题
在相同条件下,下列说法错误的是
A.氯气在饱和食盐水中的溶解度小于在纯水中的溶解度
B.NO可用排空气法进行收集
C.碳酸的酸性比硅酸强
D.SO2 的大量排放会引起酸雨
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com