
| A. | 天然气的主要成分是乙烯 | |
| B. | 天然气、沼气都属于可再生的清洁能源 | |
| C. | 石油的裂化和裂解都属于物理变化 | |
| D. | 煤干馏产生的煤焦油中含有芳香烃 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
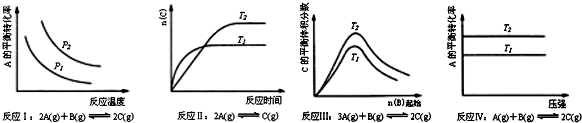
| A. | 反应Ⅰ:△H>0,P2>P1 | B. | 反应Ⅱ:△H<0,T1<T2 | ||
| C. | 反应Ⅲ:△H<0,T2>T1;或△H>0,T2<T1 | D. | 反应Ⅳ:△H<0,T2<T1或△H>0,T2>T1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 无机物不可能转化为有机物,有机物可以转化为无机物 | |
| B. | 用电子式表示氯化氢分子的形成过程: | |
| C. | 甲烷、乙醇、乙酸、苯都能发生取代反应 | |
| D. | 乙烯,丙烯,丁烯,…,聚乙烯等互为同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH值为7的溶液一定呈中性 | |
| B. | 金属材料电镀时,通常以待镀金属制品为阳极,以镀层金属为阴极 | |
| C. | 增大反应物浓度,可增大单位体积活化分子的数目,从而使反应速率增大 | |
| D. | pH=3的盐酸和pH=11的氨水溶液,溶质的浓度和导电能力均相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯可使溴水和酸性高锰酸钾溶液褪色 | |
| B. | 双氧水和SO2均可使酸性高锰酸钾溶液褪色 | |
| C. | 浓硫酸和浓盐酸暴露在空气中浓度均减小 | |
| D. | 新制氯水和SO2均可使品红褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 混合物 | 除杂试剂 | 分离方法 | |
| A | 乙酸乙酯(乙酸) | 饱和Na2CO3 | 分液 |
| B | 乙醇(乙酸) | NaOH溶液 | 分液 |
| C | 甲苯(苯酚) | 溴水 | 过滤 |
| D | 溴苯(溴) | NaOH溶液 | 蒸馏 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 尽可能使用稀溶液 | B. | 选择合适的催化剂 | ||
| C. | 增大固体反应物的表面积 | D. | 提高反应体系的温度 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 某化学兴趣小组利用FeCl2溶液与Cl2反应制取FeCl3溶液.他们按如图装置进行实验,即可制得FeCl3溶液. 请回答下列问题:
某化学兴趣小组利用FeCl2溶液与Cl2反应制取FeCl3溶液.他们按如图装置进行实验,即可制得FeCl3溶液. 请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com