
设NA表示阿伏伽德罗常数的值,下列说法中正确的 ( )
A.常温下,42 g C2H4和C4H8的混合物中含有的碳原子数为3 NA
B.58.5 g氯化钠固体中含有NA个氯化钠分子;
C.标况下,11.2 L己烷所含的分子数为0.5 NA;
D.1 mol FeCl3完全水解转化为氢氧化铁胶体后生成NA个胶粒;
科目:高中化学 来源: 题型:
已知甲、乙、丙为常见单质,A、B、C、D、E、F、G、X均为常见的化合物;B和X的摩尔质量相同,E的相对分子质量比D的相对分子质量大16。在一定条件下,各物质相互转化关系如下图所示:
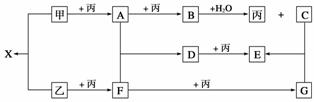
(1)写出X的电子式和G的化学式:X______________________________________,
G______________。
(2)写出有关变化的化学方程式:
B+H2O:_____________________________________________________________; D+丙:______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
有一瓶澄清的溶液,其中可能含H+、NH4+、K+、Cu2+、Fe3+、CO32-、I-中的一种或几种,取该溶液进行如下实验:
①用pH试纸检验,表明溶液呈强酸性
②取部分溶液,加入数滴新制的氯水及少量的CCl4,振荡后CCl4层显紫色
③另取部分溶液,逐滴加入稀NaOH溶液,使溶液从酸性逐渐转变为碱性,在滴加过程中及滴加完毕后,溶液中均无沉淀生成
④将③得到的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝。
根据上述实验事实确定并回答:
⑴在溶液中,肯定存在的有 ,肯定不存在的离子有 。
⑵不能确定是否存在的离子有_______。证明它(们)是否存在的实验方法是 。
⑶写出步骤②涉及的离子方程式,并用单线桥标出电子转移的方向和数目
。
⑷写出步骤④涉及的离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于氧化物的叙述正确的是
A.能和强酸溶液反应的氧化物就是碱性氧化物
B.不能跟碱反应的氧化物一定能和酸反应
C.金属氧化物一定是碱性氧化物
D.酸性氧化物不一定都能与水反应生成酸
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学兴趣小组在实验室制取漂白粉,并探究氯气与石灰乳反应的条件和产物。
已知:①二氧化锰与浓盐酸反应可制备氯气,同时生成MnCl2。
②氯气和碱的反应的过程中放出热量。温度较高时,氯气和碱还能发生如下反应:
6Cl2 + 6Ca(OH)2  5CaCl2 + Ca(ClO3)2 + 6H2O
5CaCl2 + Ca(ClO3)2 + 6H2O
该兴趣小组设计了下列实验装置,进行实验。
 |
甲 乙 丙 丁
请回答下列问题:
(1)①甲装置中发生反应的化学方程式是 。
②乙装置中的试剂是 ,作用是 。
③该兴趣小组用300mL 12mol/L盐酸与17.4g MnO2制备氯气,并将所得氯气与过量的石灰乳反应。则理论上最多可制得标况下氯气 L,Ca(ClO)2 g。
 (2)小组成员发现,产物中Ca(ClO)2的质量明显小于
(2)小组成员发现,产物中Ca(ClO)2的质量明显小于
理论值。他们讨论后认为,部分氯气未与石灰乳
反应而逸出,以及温度升高是可能原因。为了探
究反应条件对产物的影响,他们另取一定量的石
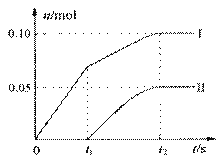
灰乳,缓慢、匀速地通入足量氯气,得出了ClO—、
ClO3— 两种离子的物质的量(n)与反应时间(t)
的关系曲线,粗略表示为右图(不考虑氯气和水
的反应)。
①图中曲线Ⅱ表示 离子的物质的量随反应时间变化的关系。
②所取石灰乳中含有Ca(OH)2的物质的量为 mol。
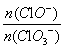 ③另取一份与②等物质的量Ca(OH)2的石灰乳,以较大的速率通入足量氯气,反应后测得产物中Cl—的物质的量为0.35mol,则产物中 = 。
③另取一份与②等物质的量Ca(OH)2的石灰乳,以较大的速率通入足量氯气,反应后测得产物中Cl—的物质的量为0.35mol,则产物中 = 。
查看答案和解析>>
科目:高中化学 来源: 题型:
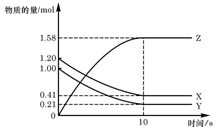
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如右图所示,下列描述正确的是 ( )
A.反应开始到10s,用Z表示的反应速率为0.158mol/(L·s)
B.反应开始到10s, X的物质的量浓度减少了0.79mol/L
C.反应开始时10s, Y的转化率为79.0%
D.反应的化学方程式为:X(g)+ Y(g) Z(g)
Z(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式与所述事实相符且正确的是( )
A.漂白粉溶液在空气中失效:ClO-+CO2+H2O=HClO+HCO3-
B.向Na2SO3溶液中通入足量氯气:SO32-+Cl2+H2O=SO42-+2Cl-+2H+
 C.用浓盐酸与MnO2反应制取少量氯气:MnO2+2H++2Cl-=Mn2++Cl2↑+2H2O
C.用浓盐酸与MnO2反应制取少量氯气:MnO2+2H++2Cl-=Mn2++Cl2↑+2H2O
D.钠与CuSO4溶液反应:2Na+Cu2+===Cu+2Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
在一密闭容器中,反应aA(g) bB(g)达平衡后,保持温度不变,将容器容积增加一倍,达到新平衡时,B的浓度是原来的60%。则下列叙述正确的是( )
bB(g)达平衡后,保持温度不变,将容器容积增加一倍,达到新平衡时,B的浓度是原来的60%。则下列叙述正确的是( )
A.a>b B. 平衡向正反应方向移动 C.A的转化率减小 D.B的质量分数减小
查看答案和解析>>
科目:高中化学 来源: 题型:
镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海 水中提取的。某学校课外兴趣小组从海水晒盐后的盐卤(主要含Na+、Mg2+、Cl-、Br-等)中模拟工业生产来提取镁,主要过程如下:
水中提取的。某学校课外兴趣小组从海水晒盐后的盐卤(主要含Na+、Mg2+、Cl-、Br-等)中模拟工业生产来提取镁,主要过程如下:
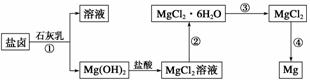
回答下列问题:
(1)工业上从盐卤中获取Mg(OH)2用石灰乳而不用NaOH溶液的原因是________________________________________________________________________。
(2)从过程①得到的Mg(OH)2沉淀中混有少量的Ca(OH)2,除去少量Ca(OH)2的方法是先将沉淀加入到盛有________溶液的烧杯中,充分搅拌后经________、______(填操作方法)可得纯净的Mg(OH)2。
(3)下图是该兴趣小组设计进行过程③的实验装置图:
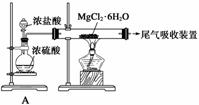
其中装置A的作用是____________________________________________________。
(4)写出过程④中发生反应的化学方程式___________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com