
| A、2013年0点钟声敲响后的几个小时,北京的污染指数从轻度污染上升为重度污染,主要污染为PM2.5污染,看来烟花爆竹的燃放,可加重PM2.5污染 |
| B、催化剂之所以能加快反应速率,是因为催化剂能降低反应的活化能 |
| C、氨气的水溶液氨水可以导电,因此氨气是电解质 |
| D、大量燃烧含硫燃料是形成酸雨的主要原因 |


科目:高中化学 来源: 题型:
| T/K | 303 | 313 | 323 | 353 |
| NH3生成量/(10-6mol) | 4.8 | 5.9 | 6.0 | 2.0 |

| 4 |
| 7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氨水使湿润的红色石蕊试纸变蓝:NH3?H2O?NH4++OH- |
| B、工业上用过量的NaOH溶液吸收SO2:SO2+OH-═HSO3- |
| C、用烧碱溶液清洗铝表面的氧化膜:2OH-+Al2O3═2AlO2-+H2O |
| D、用石灰乳吸收泄漏的氯气:2Ca(OH)2+2Cl2═CaCl2+Ca(ClO)2+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硫酸铝与过量的氨水反应:Al3++4OH-═AlO2-+2H2O | ||||
| B、除去铁粉中的铝:2Al+2NaOH═2NaAlO2+H2↑ | ||||
C、实验室制取Cl2的离子方程式:MnO2+4HCl(浓)
| ||||
D、浓硫酸与铜的反应:Cu+2H2SO4(浓)
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、b电极与电源的正极相连接 |
| B、电解过程中,水既是氧化剂又是还原剂 |
| C、a极附近溶液的pH变小 |
| D、b极的电极反应式是4OH--4e-═O2+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、酸性FeSO4溶液中加入双氧水:2Fe2++H2O2+2H+═2Fe3++2H2O | ||||
B、电解饱和MgCl2溶液:2H2O+2Cl-
| ||||
| C、向Ca(ClO)2溶液中通入SO2气体:Ca2++2ClO-+H2O+SO2═CaSO3↓+2HClO | ||||
| D、向饱和碳酸氢钙溶液中加入足量氢氧化钠溶液:Ca2++HCO3-+OH-═CaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 条件X | 变量Y | |
| a | 压强 | 反应的平衡常数 |
| b | 温度 | CO的平衡浓度 |
| c | 温度 | N2的体积分数 |
| d | 催化剂 | NO的平衡转化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
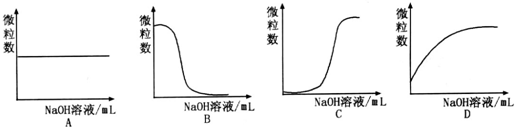
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com