
| 选项 | X(括号中的物质为杂质) | ① | ② |
| A | 乙酸乙酯(乙醇) | 饱和碳酸钠溶液 | 萃取、分液 |
| B | BaSO4(BaSO3) | 稀硝酸 | 过滤 |
| C | NaCl(Na2CO3) | 盐酸 | 蒸发结晶 |
| D | 铜(铝) | 浓硫酸 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.乙酸乙酯不溶于饱和碳酸钠溶液,乙醇易溶于水;
B.稀硝酸可氧化BaSO3生成BaSO4;
C.碳酸钠与盐酸反应生成氯化钠;
D.铝与浓硫酸发生钝化,不能除去杂质.
解答 解:A.乙酸乙酯不溶于饱和碳酸钠溶液,乙醇易溶于水,可用分液的方法分离,故A正确;
B.稀硝酸可氧化BaSO3生成BaSO4,过滤可得到硫酸钡,故B正确;
C.碳酸钠与盐酸反应生成氯化钠,蒸发结晶可得到氯化钠,故C正确;
D.常温下,铝与浓硫酸发生钝化,不能除去杂质,可用氢氧化钠溶液除杂,故D错误.
故选D.
点评 本题考查常见物质的分离、提纯,侧重于学生的分析能力和实验能力的考查,为高频考点,注意把握相关实验方法、原理和注意事项,难度不大.


 英才计划期末调研系列答案
英才计划期末调研系列答案 精英口算卡系列答案
精英口算卡系列答案科目:高中化学 来源: 题型:选择题
| A. | 25℃时,pH=13的 Ba(OH)2溶液中含有的OH-数目为0.2 NA | |
| B. | 2.24LCO和CO2的混合气体中所含的碳原子数一定是NA | |
| C. | 78g苯含有C=C双键的数目为3NA | |
| D. | 5.6 g铁和6.4 g铜分别与0.1 mol氯气完全反应,转移的电子数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
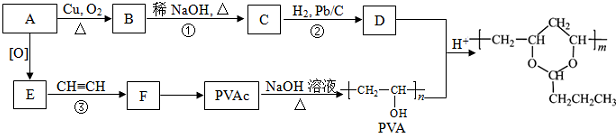
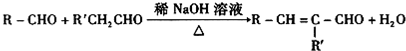
 (R、R′可表示烃基或氢原子)
(R、R′可表示烃基或氢原子)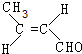 ,该分子中最多有9个原子共平面.
,该分子中最多有9个原子共平面. $→_{△}^{NaOH}$
$→_{△}^{NaOH}$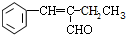 +H2O.
+H2O.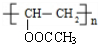 .
.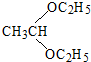 .合成路线流程图示例如下:
.合成路线流程图示例如下: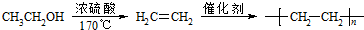
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 火碱能与酸反应,可用于治疗胃酸过多 | |
| B. | 晶体硅硬度大,可用于制作半导体材料 | |
| C. | SO2具有还原性,可用于漂白纸浆 | |
| D. | MgO、Al2O3熔点高,它们都可用于制作耐火材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
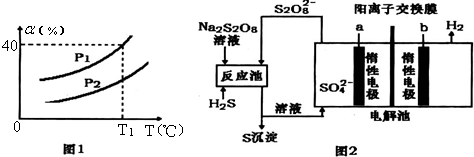
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用铜电极电解硝酸银溶液:4Ag++2H2O$\frac{\underline{\;通电\;}}{\;}$4Ag+O2↑+4H+ | |
| B. | FeS中加入足量稀硝酸:FeS+2 H+=Fe2++H2↑ | |
| C. | 石灰石溶于醋酸溶液中:CaCO3+2H+=Ca2++H2O+CO2↑ | |
| D. | 澄清石灰水中通入过量的CO2:CO2+OH-=HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X最高价氧化物对应的水化物为强酸 | |
| B. | 原子半径大小顺序为M>W>X>Y>Z | |
| C. | 水溶液中Z 的简单单核离子能促进水的电离 | |
| D. | Z、M的最高价氧化物对应的水化物均能溶解W与X形成的化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
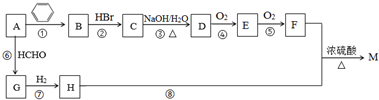
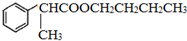 .B的一种同类别异构体存在顺反异构,该物质发生加聚反应生成的高分子化合物的结构简式为
.B的一种同类别异构体存在顺反异构,该物质发生加聚反应生成的高分子化合物的结构简式为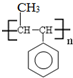 .
.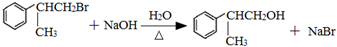 .
.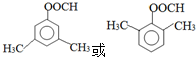 (任写一种物质的结构简式).
(任写一种物质的结构简式).查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 ; NH3的VSEPR模型为正四面体;请解释加入乙醇后析出晶体的原因乙醇分子的极性比水弱,由于减小溶剂的极性,降低离子化合物Cu(NH3)4SO4•H2O的溶解度.
; NH3的VSEPR模型为正四面体;请解释加入乙醇后析出晶体的原因乙醇分子的极性比水弱,由于减小溶剂的极性,降低离子化合物Cu(NH3)4SO4•H2O的溶解度. .乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高得多,原因是乙二胺分子间存在氢键而三甲胺没有,由于氢键的作用力比范德华力大,故乙二胺沸点比三甲胺高.
.乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高得多,原因是乙二胺分子间存在氢键而三甲胺没有,由于氢键的作用力比范德华力大,故乙二胺沸点比三甲胺高.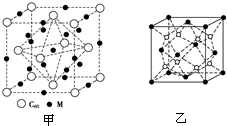
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com