


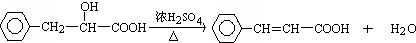 .
. .
. .
. 、
、 .
. (其中X、Y均部位H)
(其中X、Y均部位H)分析 根据A是苯乙烯可知,A与水发生加成反应得B为苯乙醇,B氧化得C为苯乙醛,C发生题中信息②的反应可得D为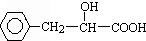 ,F为含有三个六元环的酯,D发生酯化反应得F为
,F为含有三个六元环的酯,D发生酯化反应得F为 ,D发生消去反应得G为:
,D发生消去反应得G为: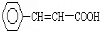 ,D发生缩聚反应得E为
,D发生缩聚反应得E为 ,
,
G和甲醇酯化反应得H 为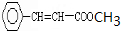 ,H发生加聚反应得
,H发生加聚反应得 ,据此答题.
,据此答题.
解答 解:根据A是苯乙烯可知,A与水发生加成反应得B为苯乙醇,B氧化得C为苯乙醛,C发生题中信息②的反应可得D为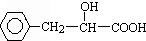 ,F为含有三个六元环的酯,D发生酯化反应得F为
,F为含有三个六元环的酯,D发生酯化反应得F为 ,D发生消去反应得G为:
,D发生消去反应得G为: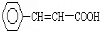 ,D发生缩聚反应得E为
,D发生缩聚反应得E为 ,
,
G和甲醇酯化反应得H 为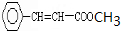 ,H发生加聚反应得
,H发生加聚反应得 ,
,
(1)根据上面的分析可知,D→G的反应类型是消去产物,H是G和甲醇酯化反应的产物,
故答案为:消去反应;酯化反应(或取代反应);
(2)G是D的消去产物,G为: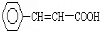 ,故D转化为G的化学方程式是:
,故D转化为G的化学方程式是: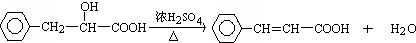 ,
,
故答案为: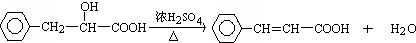 ;
;
(3)E是D的缩聚产物,化学方程式是  ,
,
故答案为: ;
;
(4)根据上面的分析可知,F结构简式是  ,
,
故答案为: ;
;
(5)能发生银镜反应,说明含有醛基,能使FeCl3溶液呈紫色,说明含有酚羟基,故结构简式有: 、
、 ,
,
故答案为: 、
、 .
.
点评 本题是一道有机框图推断题,要掌握官能团决定的物质的性质,是现在高考的热点和难点,难度中等.


科目:高中化学 来源: 题型:填空题
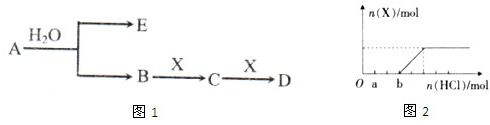
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入NH4HSO4固体,v(H2)不变 | B. | 加入少量硫酸钠溶液,v(H2)减小 | ||
| C. | 加入CH3COONa固体,v(H2)不变 | D. | 滴加少量CuSO4溶液,v(H2)减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
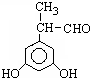
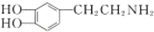 是一种重要的中枢神经传导物质,是用来帮助细胞传送脉冲的化学物质,能影响人对事物的欢愉感受,多巴胺可由D(香兰素)与硝基甲烷反应后再经锌汞齐还原水解制得.合成过程如图所示:
是一种重要的中枢神经传导物质,是用来帮助细胞传送脉冲的化学物质,能影响人对事物的欢愉感受,多巴胺可由D(香兰素)与硝基甲烷反应后再经锌汞齐还原水解制得.合成过程如图所示:
 +H2$\stackrel{催化剂}{→}$
+H2$\stackrel{催化剂}{→}$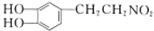 .
.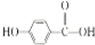 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 还原性:Br->Fe2+>I- | B. | 还原性:I->Fe2+>Br- | ||
| C. | 氧化性:Br2>I2>Fe3+ | D. | 氧化性:I2>Fe3+>Br2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | n-2 | B. | n | C. | n-1 | D. | 2n |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com