
| A、任何能使熵值减小的过程都能自发进行 | B、1mol NaOH分别和1mol CH3COOH、1mol HNO3反应,后者比前者△H小 | C、已知热化学方程式2SO2(g)+O2(g)?2SO3(g);△H=-Q kJ?mol-1(Q>0),则将2mol SO2(g)和1 mol O2(g)置于一密闭容器中充分反应后放出Q kJ的热量 | D、在Na2SO4溶液中加入过量的BaCl2后,溶液中不存在SO42- |


科目:高中化学 来源: 题型:
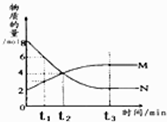 在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )| A、反应的化学方程式为:N?2M | B、t2时,反应不再发生 | C、t2时,正反应速率等于逆反应速率 | D、t3后,反应到达最大限度 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com