
| A. | 0.5mol Mg与足量盐酸反应生成氢气的体积为11.2升 | |
| B. | 标准状况下,11.2L SO2所含的原子数为1.5NA | |
| C. | 8gCH4所含的氢原子数为0.5NA | |
| D. | 46g NO2和N2O4的混合物所含的分子数为1NA |
分析 A.没有告诉在标准状况下,不能使用标况下的气体摩尔体积计算;
B.根据n=$\frac{V}{{V}_{m}}$计算出二氧化硫的物质的量,然后计算出含有原子的物质的量及数目;
C.根据n$\frac{m}{M}$计算出甲烷的物质的量,然后可计算出含有原子的物质的量及数目;
D.NO2和N2O4的摩尔质量不同,无法计算混合物中含有分子数.
解答 解:A.不是标况下,不能使用标准状况下的气体摩尔体积计算生成氢气的体积,故A错误;
B.标准状况下,11.2L SO2的物质的量为:$\frac{11.2L}{22.4L/mol}$=0.5mol,0.5mol二氧化硫含有1.5mol原子,含有的原子数为1.5NA,故B正确;
C.8gCH4的物质的量为:$\frac{8g}{16g/mol}$=0.5mol,0.5mol甲烷中含有氢原子的物质的量为:0.5mol×4=2mol,含有氢原子数为2NA,故C错误;
D.NO2和N2O4的摩尔质量分别为46g/mol、92g/mol,无法计算46g混合物的物质的量及含有分子数,故D错误;
故选B.
点评 本题考查阿伏加德罗常数的综合应用,题目难度中等,注意明确标况下气体摩尔体积的使用条件,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,试题有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
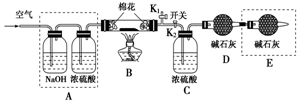 为探究所得的水合碱式碳酸镁[mMgCO3•nMg(OH)2•x
为探究所得的水合碱式碳酸镁[mMgCO3•nMg(OH)2•x查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (1)(2)(3)(5) | B. | (1)(3)(5) | C. | (2)(3)(6) | D. | (1)(3)(4)(5) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在0.1mol/LNaHCO3溶液中:Al3+、NH4+、SO42-、NO3- | |
| B. | 常温下,$\frac{{K}_{W}}{c({H}^{+})}$=0.1mol/L的溶液中:K+,Cl-,Fe2+,NO3- | |
| C. | 使甲基橙变红的溶液中:NH4+,Cl-,SO2-,Mg2+ | |
| D. | 25℃时,水电离出的c(H+)=1×10-13mol/L:K+,Ba2+,NO3-,S2- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯的三氯代物一共有 5 种 | |
| B. | 乙烯和乙酸均能发生加成反应 | |
| C. | 乙烷通入氯水中能发生取代反应 | |
| D. | 淀粉和纤维素都属于天然高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用小苏打治疗胃酸过多:HCO3-+H+═CO2↑+H2O | |
| B. | 纯碱溶液与石灰水反应:Ca2++CO32-=CaCO3↓ | |
| C. | 铜粉与硝酸银溶液反应:Ag++Cu═Ag+Cu2+ | |
| D. | 盐酸滴在石灰石上:CaCO3+2H+=Ca2++CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可用磨口玻璃瓶保存NaOH溶液 | |
| B. | 使用容量瓶配制100g 36%的NaCl溶液 | |
| C. | 稀硝酸可除去试管内壁的银镜 | |
| D. | 加热可除去NaHCO3固体中混有的Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 200mL0.5mol/LNaCl溶液 | B. | 100mL0.8mol/LNaBr溶液 | ||
| C. | 800mL0.3mol/LNa2CO3溶液 | D. | 1000mL0.6mol/LNaNO3溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com