
【题目】具有解热镇痛及抗生素作用的药物“芬必得”主要成分的结构简式为
 ,它属于
,它属于
A. 芳香烃B. 易溶于水的有机物C. 苯甲酸的同系物D. 高分子化合物
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】实验小组进行如下实验:
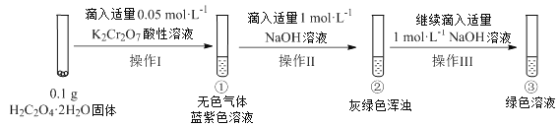
已知:Cr2(SO4)3稀溶液为蓝紫色;Cr(OH)3为灰绿色固体,难溶于水。
下列关于该实验的结论或叙述不正确的是
A. ①中生成蓝紫色溶液说明K2Cr2O7在反应中表现了氧化性
B. 若继续向③中加入稀硫酸,溶液有可能重新变成蓝紫色
C. 将①与③溶液等体积混合会产生灰绿色浑浊,该现象与Cr3+的水解平衡移动有关
D. 操作I中产生的无色气体是CO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。下表列出了a~f6元素在周期表中的位置。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
一 | ||||||||
二 | a | b | ||||||
三 | c | d | e | f |
回答下列问题
(1)写出a单质的电子式________。
(2)画出b的原子结构示意图:__________。
(3)写出c单质和水反应的化学方程式:__________。
(4)金属性c强于
(5)已知硒(Se)与e同主族,且位于e的下一个周期,根据硒元素在元素周期表中的位置推测硒及其化合物可能具有的性质是______。
①最高价氧化物对应的水化物的化学式为H2SeO3
②SeO2既有氧化性又有还原性
③气态氢化物的稳定性比e元素的弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨对人类的生存和发展有着重要意义,1909年哈伯在实验室中首次利用氮气与氢气反应合成氨,实现了人工固氮。
(1)反应N2(g) + 3H2(g) ![]() 2NH3(g)的化学平衡常数表达式为______。
2NH3(g)的化学平衡常数表达式为______。
(2)请结合下列数据分析,工业上选用氮气与氢气反应固氮,而没有选用氮气和氧气反
应固氮的原因是______。
序号 | 化学反应 | K(298K)的数值 |
① | N2(g) + O2(g) | 5×10-31 |
② | N2(g) + 3H2(g) | 4.1×106 |
(3)对于反应N2(g)+3H2(g)![]() 2NH3(g),在一定条件下氨的平衡含量如下表。
2NH3(g),在一定条件下氨的平衡含量如下表。
温度/℃ | 压强/MPa | 氨的平衡含量 |
200 | 10 | 81.5% |
550 | 10 | 8.25% |
① 该反应为______(填“吸热”或“放热”)反应。
② 其他条件不变时,温度升高氨的平衡含量减小的原因是______(填字母序号)。
a. 温度升高,正反应速率减小,逆反应速率增大,平衡逆向移动
b. 温度升高,浓度商(Q)变大,Q > K,平衡逆向移动
c. 温度升高,活化分子数增多,反应速率加快
d. 温度升高,K变小,平衡逆向移动
③ 哈伯选用的条件是550℃、10 MPa,而非200℃、10 MPa,可能的原因是______。
(4)一定温度下,在容积恒定的密闭容器中充入1 mol 氮气和3 mol氢气,一段时间后达化学平衡状态。若保持其他条件不变,向上述平衡体系中再充入1 mol氮气和3 mol 氢气,氮气的平衡转化率______(填“变大”“变小”或“不变”)。
(5)尽管哈伯的合成氨法被评为“20世纪科学领域中最辉煌的成就”之一,但仍存在耗能高、产率低等问题。因此,科学家在持续探索,寻求合成氨的新路径。下图为电解法合成氨的原理示意图,阴极的电极反应式为______。
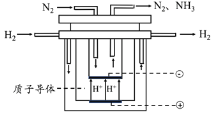
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】周期表前四周期的元素![]() 、
、![]() 、
、![]() 、
、![]() ,原子序数依次增大,X原子基态时
,原子序数依次增大,X原子基态时![]() 层中
层中![]() 轨道电子数与s轨道电子数相同;
轨道电子数与s轨道电子数相同;![]() 原子基态时2p原子轨道上有3个未成对的电子;Z有多种氧化物,其中一种红棕色氧化物可作涂料;
原子基态时2p原子轨道上有3个未成对的电子;Z有多种氧化物,其中一种红棕色氧化物可作涂料;![]() 位于第四周期,其原子最外层只有1个电子,且内层都处于全充满状态。回答下列问题:
位于第四周期,其原子最外层只有1个电子,且内层都处于全充满状态。回答下列问题:
(1)X位于周期表的第_______周期,第______族。
(2)元素的第一电离能:X______Y(填“>”或“<”,下同);原子半径:X______Y。
(3)![]() 的最高价氧化物对应水化物中酸根离子的空间构型是_______(用文字描述)。
的最高价氧化物对应水化物中酸根离子的空间构型是_______(用文字描述)。
(4)![]() 基态核外电子排布式为_________,用铁氰化钾溶液检验
基态核外电子排布式为_________,用铁氰化钾溶液检验![]() 的离子方程式为___________。
的离子方程式为___________。
(5)元素W的一种氯化物晶体的晶胞结构如图所示,该氯化物的化学式是_______,它可与浓盐酸发生非氧化还原反应,生成配合物![]() ,反应的化学方程式:_________。
,反应的化学方程式:_________。
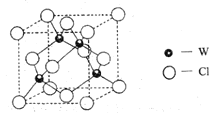
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】资源化利用![]() ,不仅可以减少温室气体的排放,还可以获得燃料或重要的化工产品。
,不仅可以减少温室气体的排放,还可以获得燃料或重要的化工产品。
(1)![]() 的捕集:
的捕集:
①![]() 属于___________分子(填“极性”或“非极性”),其晶体(干冰)属于__________晶体。
属于___________分子(填“极性”或“非极性”),其晶体(干冰)属于__________晶体。
②用饱和![]() 溶液做吸收剂可“捕集”
溶液做吸收剂可“捕集”![]() 。若所得溶液
。若所得溶液![]() ,溶液中
,溶液中![]() _______;(室温下,
_______;(室温下,![]() 的
的![]() )若吸收剂失效,可利用
)若吸收剂失效,可利用![]() 溶液使其再生,写出该反应的离子方程式_____。
溶液使其再生,写出该反应的离子方程式_____。
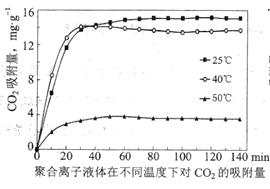
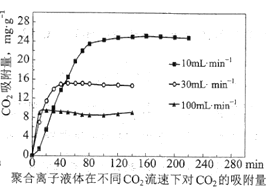
③聚合离子液体是目前广泛研究的![]() 吸附剂。结合下图分析聚合离子液体吸附
吸附剂。结合下图分析聚合离子液体吸附![]() 的有利条件是____________。
的有利条件是____________。
(2)生产尿素:工业上以![]() 、
、![]() 为原料生产尿素
为原料生产尿素![]() ,该反应分为二步进行:
,该反应分为二步进行:
第一步:![]()
![]()
第二步:![]()
![]()
写出上述合成尿素的热化学方程式_______。
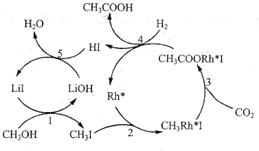
(3)合成乙酸:中国科学家首次以![]() 、
、![]() 和
和![]() 为原料高效合成乙酸,其反应路径如图所示:
为原料高效合成乙酸,其反应路径如图所示:
①原料中的可通过电解法由![]() 制取,用稀硫酸作电解质溶液,写出生成
制取,用稀硫酸作电解质溶液,写出生成![]() 的电极反应式:____________。
的电极反应式:____________。
②根据图示,写出总反应的化学方程式:_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】德国化学家哈伯(F.Haber)从1902年开始研究由氮气和氢气直接合成氨。合成氨为解决世界的粮食问题作出了重要贡献。其原理为N2(g)+3H2(g)2NH3(g) △H=-92.4kJ/mol
(1)若已知H-H键的键能为436.0kJ/mol,N-H的键能为390.8kJ/mol,则N![]() N的键能约为_____kJ/mol
N的键能约为_____kJ/mol
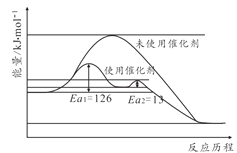
(2)合成氨反应不加催化剂很难发生,催化剂铁触媒加入后参与了反应降低了活化能。其能量原理如图所示,则加了催化剂后整个反应的速率由______决定(填“第一步反应”或者“第二步反应”),未使用催化剂时逆反应活化能______正反应活化能(填“大于”“小于”或者“等于”)
(3)从平衡和速率角度考虑,工业生产采取20MPa到50MPa的高压合成氨原因______
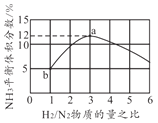
(4)一定温度下恒容容器中,以不同的H2和N2物质的量之比加入,平衡时NH3体积分数如图所示,则H2转化率a点______b点(填"大于”“小于”或者“等于”)。若起始压强为20MPa,则b点时体系的总压强约为______MPa。
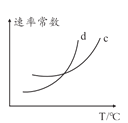
(5)若该反应的正逆反应速率分别表示为v正=K正![]() ,v逆=K逆c2(NH3),则一定温度下,该反应 的平衡常数K=______(用含K正和K逆的表达式表示),若K正和K逆都是温度的函数,且随温度升高而升高,则图中c和d分别表示______和______随温度变化趋势(填K正或者K逆)。
,v逆=K逆c2(NH3),则一定温度下,该反应 的平衡常数K=______(用含K正和K逆的表达式表示),若K正和K逆都是温度的函数,且随温度升高而升高,则图中c和d分别表示______和______随温度变化趋势(填K正或者K逆)。
(6)常温下,向20mL的0.1mol/L的盐酸中通入一定量氨气反应后溶液呈中性(假设溶液体积变化忽略不计)则所得溶液中c(NH4+)=_______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释事实的离子方程式不正确的是( )
A.水玻璃中滴入酚酞呈红色:SiO32-+2H2O ![]() H2SiO3+2OH-
H2SiO3+2OH-
B.Ba(NO3)2溶液中通入过量SO2:3SO2+ 3Ba2++ 2NO3- + 2H2O= 3BaSO4↓ + 2NO↑ + 4H+
C.NH4Al(SO4)2溶液中滴入过量NaOH溶液:NH4++Al3++5OH-=Al(OH)4- +NH3·H2O
D.AgNO3溶液中滴入足量氨水中:Ag++2NH3·H2O=Ag(NH3)2++2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com