

【题目】某学习小组在实验室制取CO2气体的过程中,不慎用到了浓盐酸,导致制得的CO2气体中混有HCl气体,他们设计了如下除去HCl气体并探究CO2与过氧化钠(Na2O2)反应的实验。请回答下列问题:
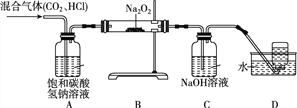
(1)装置A的作用是___________________________。
(2)为确定反应后装置B硬质玻璃管中固体的成分,小组同学取适量固体于试管中,加入足量的蒸馏水溶解形成溶液M,无气泡产生,则该固体中不含________,该小组同学继续进行探究。
【提出问题】反应后硬质玻璃管中固体的成分是什么?
(3)【做出猜想】猜想一:Na2CO3;猜想二:NaOH;猜想三:Na2CO3和NaOH
经过讨论,大家一致认为猜想二不合理,理由是_____________________________(用化学反应方程式表示)。
(4)【实验验证】小组同学取上述形成的溶液M于试管中,向其中加入过量的____________________溶液,若产生白色沉淀,过滤,向滤液中滴加几滴酚酞试液,溶液变红,则证明猜想三成立。
(5)【交流反思】小组中有同学认为,将上述滤液中滴加的酚酞试液换成硝酸铜溶液,也能得出同样的结论,你认为该同学的观点_____________(填“正确”或“错误”),理由是:____________________________________________(用化学反应方程式表示)。
【答案】 吸收CO2中混有的HCl Na2O2 2CO2+2Na2O2===2Na2CO3+O2或CO2+2NaOH===Na2CO3+H2O BaCl2或Ba(NO3)2或CaCl2或Ca(NO3)2 正确 Cu(NO3)2+2NaOH===Cu(OH)2↓+2NaNO3
【解析】试题分析:由题意及实验装置可知,A装置用于除去二氧化碳中的氯化氢杂质,B中潮湿的二氧化碳与过氧化钠反应,C装置用于吸收剩余的二氧化碳,D装置用于收集氧气。
(1)装置A的作用是吸收CO2中混有的HCl。
(2)为确定反应后装置B硬质玻璃管中固体的成分,小组同学取适量固体于试管中,加入足量的蒸馏水溶解形成溶液M,无气泡产生,因为Na2O2可以与水反应生成氧气,所以该固体中不含Na2O2。
(3)猜想二不合理,理由是二氧化碳与过氧化钠反应生成碳酸钠和氧气,水蒸气与过氧化钠反应,虽然能生成氢氧化钠,但是氢氧化钠可以与二氧化碳继续反应生成碳酸钠,化学方程式为2CO2+2Na2O2===2Na2CO3+O2或CO2+2NaOH===Na2CO3+H2O。
(4)取上述溶液M于试管中,向其中加入过量的BaCl2(或Ba(NO3)2或CaCl2或Ca(NO3)2)溶液,若产生白色沉淀,过滤,向滤液中滴加几滴酚酞试液,溶液变红,则证明反应后的固体为Na2CO3和NaOH,猜想三成立。
(5)将上述滤液中滴加的酚酞试液换成硝酸铜溶液,也能得出同样的结论,该同学的观点是正确的,理由是向滤液中滴加硝酸铜溶液后,若溶液中有蓝色沉淀生成,则可证明滤液中含有氢氧化钠,化学反应方程式为Cu(NO3)2+2NaOH===Cu(OH)2↓+2NaNO3。


 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案科目:高中化学 来源: 题型:
【题目】我国产铜主要取自黄铜矿(CuFeS2),湿法炼铜工艺的核心是黄铜矿的浸出,目前主要有氧化浸出、配位浸出和生物浸出三种方法。
I.氧化浸出
(1)在硫酸介质中用双氧水将黄铜矿氧化,测得有SO42-生成。
①该反应的离子方程式为________________________________.
②该反应在25—50℃下进行,实际生产中双氧水的消耗量要远远高于理论值,试分析其原因为__________________________________________________
Ⅱ,配位浸出
反应原理为:CuFeS2+NH3·H2O+O2+OH-→ Cu(NH3)42++Fe2O3+SO42-+H2O(未配平)
(2)用化学用语解释氨水溶液的酸碱性______________________________.
(3)生产中为了稳定溶液的pH,可以在浸出液加入___________________(物质名称)Ⅲ.生物浸出
在反应釜中加入黄铜矿、硫酸铁、硫酸和微生物,并鼓入空气,黄铜矿逐渐溶解,反应釜中各物质的转化关系如图所示。
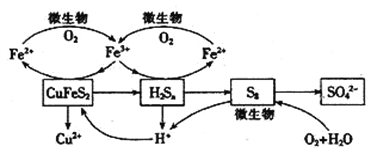
(4)在微生物的作用下,可以循环使用的物质有_________(填化学式),微生物参与的离子反应方程式为_______________________________(任写一个)。
(5)假如黄铜矿中的铁元素最终全部转化为Fe3+,当有2 mol SO42-生成时,理论上消耗O2的物质的量为_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分。
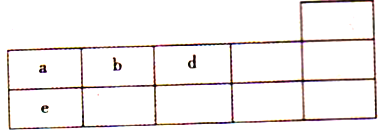
(1)a原子结构示意图为___________,d的一种氢化物为常见溶剂,其电子式为__________。
(2)e的最高价氧化物对应水化物的钠盐液中通入少量a的最高价氧化物会发生反应,写出相应的离子方程式:____________________________________。
(3)X、Y为同周期元素,它们简单离子的电子层与d离子的电子层结构相同,Y离子半径在同周期元素简单离子半径中最小,X、Y两种元素最高价氧化物对应的水化物之间可以相互反应生成盐和水,写出该反应的化学方程式:____________________________,X在周期表中的位置为________________。
(4)与Y同周期的W元素,其原子半径是同周期主族元素中最小的。工业上制取Y和W的无水化合物方法如下:Y的氧化物与a、W的单质在高温条件下反应,每消耗6kg a的单质,过程中转移1×103mol电子,写出相应反应的化学方程式:_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“雾霾”“PM2.5”已成为电视、新闻热词,下列做法不符合“环境友好”的是( )
A.使用清洁能源,减少煤的燃烧
B.减轻交通压力,提倡私家车出行
C.道路、建筑工地定期喷洒水,减少扬尘
D.种植沙漠防护林,减少沙尘暴
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各物质的转化关系如下图所示.B、D是气体,其中B是空气的主要成分之一;C是淡黄色固体,常用于供氧剂;E是红棕色固体;F是最常见的无色液体.

回答下列问题:
(1)C的化学式是_______________.
(2)气体D通入紫色石蕊溶液的现象是_____________________.
(3)写出反应①的离子方程式______________________________________.
(4)写出反应②的化学方程式_____________________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质间的转化,通过一步反应不能实现的是( )
A.CO2→Na2CO3
B.FeCl3→FeCl2
C.H2SiO3→Na2SiO3
D.S→SO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的( )
A.钠与水的反应:2Na+2H2O═2Na++2OH﹣+H2↑
B.硅酸钠溶液中通入过量CO2:SiO ![]() +2CO2+2H2O═H2SiO3↓+2HCO3﹣
+2CO2+2H2O═H2SiO3↓+2HCO3﹣
C.氯气与水反应:Cl2+H2O═2H++Cl﹣+ClO﹣
D.明矾溶液中加入过量的Ba(OH)2溶液:Al3++4OH﹣═AlO2﹣+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作均要用玻璃棒,其中玻璃棒作用相同的是( )
① 过滤 ② 蒸发 ③ 溶解 ④ 向容量瓶中转移液体
A.①和②B.①和③C.③和④D.①和④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com