
| A. | 最高化合价按X、Y、Z的顺序减小 | B. | 阴离子的还原性按X、Y、Z顺序增强 | ||
| C. | 单质的氧化性按X、Y、Z顺序增强 | D. | 氢化物的稳定性按X、Y、Z顺序减小 |
分析 X、Y、Z元素的原子具有相同的电子层数,所以为同周期元素,这几种元素的原子序数依次增大,同一周期元素,其最高价氧化物对应水化物酸性依次增强,则非金属性X<Y<Z.
A.均存在最高价含氧酸,同周期元素中原子序数越大,最高化合价依次增大;
B.元素的非金属性增强,阴离子的还原性越弱;
C.元素的非金属性增强,其单质的氧化性越强;
D.元素的非金属性增强,形成的气态氢化物的稳定性越强.
解答 解:X、Y、Z元素的原子具有相同的电子层数,所以为同周期元素,原子序数依次增大,其最高价氧化物对应水化物酸性依次增强,则非金属性X<Y<Z.
A.均存在最高价含氧酸,故同周期元素中,原子序数越大,最高化合价依次增大,即最高正化合价按X、Y、Z的顺序增大,故A错误;
B.X、Y、Z元素的非金属性依次增强,其阴离子的还原性逐渐减弱,故B错误;
C.X、Y、Z元素的非金属性依次增强,其单质的氧化性依次增强,故C正确;
D.X、Y、Z元素的非金属性依次增强,故其氢化物越稳定性依次增强,故D错误;
故选C.
点评 本题考查结构位置性质的关系等,明确元素周期律是解本题关键,难度不大.


 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案科目:高中化学 来源: 题型:选择题
| A. | 用不活泼金属铜作电极电解饱和食盐水:2Cl-+2H2O═Cl2↑+H2↑+2OH- | |
| B. | HCO3-离子水解方程式:HCO3-+H2O═H3O++CO32- | |
| C. | 乙烯通入溴水中:C2H4+Br2═CH2BrCH2Br | |
| D. | 氯化铁溶液与碳酸氢钠溶液混合:Fe3++3HCO3-═Fe(OH)3↓+3CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通入CH4 的电极为正极 | |
| B. | 正极的电极反应式为:2O2+8e-+4H2O═8OH- | |
| C. | 若甲烷通入量为1.12 L(标准状况)且反应完全,则电池中有0.1 mol O2 被氧化 | |
| D. | 通入甲烷的电极的电极反应式为:CH4+2O2+4e-═CO2+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 容器内气体混合物的密度不随时间变化 | |
| B. | 容器内X、Y、Z的浓度之比为1:2:2 | |
| C. | 单位时间内消耗0.1mol X,同时生成0.2mol Y | |
| D. | 单位时间内消耗0.1mol X,同时生成0.2mol Z |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 测定某浓度盐酸的pH时,先将pH试纸用蒸馏水湿润 | |
| B. | 容量瓶用蒸馏水洗净、必须烘干后才能用于溶液的配制 | |
| C. | 用苯萃取溴水中的溴之后进行分液时,水层从分液漏斗的下口放出 | |
| D. | 中和滴定时,锥形瓶不需要用待测液润洗后就能使用 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:解答题
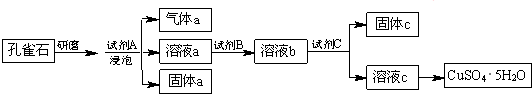
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 被提纯的物质 | 除杂试剂 | 分离方法 |
| A | 己烷(己烯) | 溴水 | 分液 |
| B | 淀粉溶液(NaCl) | 水 | 渗析 |
| C | CH3CH2OH (CH3COOH) | CaO | 蒸馏 |
| D | 肥皂(甘油) | NaCl | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室制溴苯时选用的试剂可以是溴水、苯和铁屑 | |
| B. | 配制银氨溶液时,将氨水逐滴加到 AgNO3溶液中,边加边振荡,直至沉淀恰好完全消失 | |
| C. | 将乙醇和浓硫酸按体积比1:3混合加热到170℃制乙烯 | |
| D. | 实验室制乙炔时,为了减慢反应速率,可用饱和食盐水代替蒸馏水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com